| |||
| |||
Η λεπτή υφή του αστροκυττώματος
ΜΠΑΛΟΓΙΑΝΝΗΣ I, ΒΛΑΧΑΚΗ Κ, ΚΩΣΤΑ Β, ΜΠΑΛΟΓΙΑΝΝΗΣ Σ.
Α' Νευρολογική Κλινική Νοσοκομείου ΑΧΕΠΑ Αριστοτέλειο Πανεπιστήμιο Θεσσαλονίκης
Περίληψη
Το Αστροκύττωμα είναι ένας από τους συνήθεις όγκους του ΚΝΣ. Η πορεία του
μπορεί να είναι σταθερή ή να εξελιχθεί τελικά σε Πολύμορφο Γλοιοβλάστωμα.
Στη μελέτη του όγκου υπό το ηλεκτρονικό μικροσκόπιο περιγράφουμε τις αλλοιώσεις των οργανυλίων του οι οποίες δύνανται να αποτελέσουν κριτήρια της συμπεριφοράς του όγκου και της πορείας του προς την κακοήθεια.
Σε ευρεία σειρά αστροκυττωμάτων επισημαίνονται ως κριτήρια αναπλαστικότητας:
α) οι μορφολογικές αλλοιώσεις των μιτοχονδρίων
β) η κατάσταση του λείου ενδοπλασματικού δικτύου και της συσκευής του Golgi
γ) η μεταβολή της πυκνότητας των νευρογλοιακών ινών εντός του περικαρύου
δ) η κατάτμηση των μικροσωληναρίων
ε) η πολυμορφία του πυρήνος και οι ενδοπυρηνικές εκκολπώσεις
στ) η πληθώρα των αστροκυτταρικών προσεκβολών που προβάλλουν εντός του νευροπιλημματικού χώρου ή εντός του διάμεσου ιστικού χώρου.
Τα ανωτέρω κριτήρια έχουν διαγνωστική βαρύτητα συμπληρώνοντας το διαγνωστικό φάσμα, το συνιστάμενο εξ ανοσοιστοχημικών κριτηρίων.
Εισαγωγή
Τα αστροκυττώματα αποτελούν τον συχνότερο ενδοπαρεγχυματικό όγκο του εγκεφάλου. Στις ΗΠΑ υπολογίζονται περίπου 12.000 νέες περιπτώσεις κάθε χρόνο1.
Οι όγκοι αυτοί χαρακτηρίζονται από ιδιαίτερα μεγάλη πολυμορφία και ετερογένεια και ανήκουν στα πλαίσια ενός ευρύτατου φάσματος νεοπλασμάτων που στο ένα άκρο ανευρίσκονται καλοήθεις όγκοι όπως το αργά αναπτυσσόμενο νεανικό πιλοκυτταρικό αστροκύττωμα και στο άλλο άκρο το ιδιαίτερα μεγάλης κακοήθειας πολύμορφο γλοιοβλάστωμα2.
Η κυριαρχία ενός κυτταρικού τύπου στους όγκους αυτους μας επιτρέπει μία αδρή διάκριση σε «συνήθη αστροκυττώματα» όπου ανήκουν τα ινώδη, τα γεμιστοκυτταρικά και τα πρωτοπλασματικά αστροκυττώματα και σε "ειδικούς τύπους" όπως το πιλοκυτταρικό και το κυστικό αστροκύττωμα της παρεγκεφαλίδος, που παρ' ότι εμφανίζονται σε άτομα μικρότερης ηλικίας έχουν καλύτερη βιολογική συμπεριφορά, σπάνια εμφανίζουν στοιχεία κακοήθειας και ακόμη και όταν σε αυτά εντοπίζονται τα κριτήρια κακοήθειας των «συνήθων» αστροκυττωμάτων αυτά δεν προκαθορίζουν την πρόγνωση1,3,4.
Στην έναρξη του ευρέος φάσματος των «συνήθων» αστροκυττωμάτων βρίσκεται το ινιδώδες αστροκύττωμα. Πρόκειται για έναν καλοήθη όγκο που στους ενήλικες εντοπίζεται κυρίως στα ημισφαίρια ενώ στα παιδιά συνήθως στη γέφυρα5,6. Συνήθως τα αστροκυττώματα προκαλούν ως αρχικά συμπτώματα κεφαλαλγίες και επιληπτικές κρίσεις που όχι σπάνια ταλαιπωρούν τον ασθενή για μεγάλο διάστημα μέχρι να εντοπισθεί και απεικονισθεί ο όγκος ώστε να τεθεί η τελική διάγνωση7,8,9.
Το φάσμα έρχονται να συμπληρώσουν το Αναπλαστικό Αστροκύττωμα και το επιθετικότατο Πολύμορφο Γλοιοβλάστωμα σε συχνότητα που αντιστοιχεί ανάλογα 2 προς 3 προς 51.
Τα αστροκυττώματα χαρακτηρίζονται από την ιδιαίτερη πολυμορφία της βιολογικής τους συμπεριφοράς και της φυσικής τους εξέλιξης. Κάποια εμφανίζονται ως καλοήθη και παραμένουν καλοήθη για πάρα πολλά χρόνια, κάποια αρχίζουν ως καλοήθεις όγκοι και με το χρόνο εμφανίζουν χαρακτήρες αναπλασίας ενώ κάποια έχουν μία σταθερή πορεία προς την κακοήθεια.
Η κακοήθης εξαλλαγή που επισυμβαίνει στο 50% με 70% των αστροκυττωμάτων είναι ένα ενδογενές φαινόμενο των όγκων αυτών, συμβαίνει αυτόματα και δεν έχει μέχρι πρόσφατα τουλάχιστο αναγνωρισθεί κάποιος υπεύθυνος εξωγενής παράγοντας9,10,11.
Αυτή η υποτροπή σε μια μορφή όγκου υψηλότερου βαθμού κακοήθειας, η μετεξέλιξη δηλαδή σε Αναπλαστικό Αστροκύττωμα ή Πολύμορφο Γλοιοβλάστωμα λαμβάνει χώρα εντός ενός χρονικού διαστήματος που ποικίλλει πολύ έχοντας έναν μέσο όρο τα 4,5 χρόνια12 και αποτελεί την κύρια αιτία θανάτου ενός ασθενούς που πάσχει από αστροκύττωμα13,14.
Η ταχεία εντόπιση και ο ακριβής ιστοπαθολογικός προσδιορισμός περιοχών αναπλασίας έχουν βαρύνουσα σημασία δεδομένου ότι η ριζική και ευρεία αφαίρεση του όγκου επιρρεάζει, στα low grade αστροκυττώματα, θετικά την πρόγνωση13-18.
Υλικό - Μέθοδος
Υπό το ηλεκτρονικό μικροσκόπιο μελετήθηκε ευρεία σειρά βιοψικού υλικού διεγνωσμένων low grade αστροκυττωμάτων. Τα ιστολογικά παρασκευάσματα εξετάσθηκαν αρχικώς στο οπτικό μικροσκόπιο προς εντοπισμό των υπόπτων αναπλασίας περιοχών.
Έγινε αρχική μονιμοποίηση σε διάλυμμα Sotelo το οποίο συνίσταται εκ 2,5% γλουταραλδεΰδης, 1% παραφορμαλδεΰδης και λίγων σταγόνων χλωριούχου ασβεστίου εντός ρυθμιστικού διαλύματος κακοδυλικού νατρίου όπου σταθεροποιήθηκε σε pΗ 7,35. Ακολούθησε μονιμοποίηση σε διάλυμα τετροξειδίου του οσμίου και διαδοχικές αφυδατώσεις σε διαλύματα αιθυλικής αλκοόλης και οξειδίου του προπυλενίου. Κατόπιν συσκευάσθηκαν σε κύβους αραλδίτη και ετμήθησαν αρχικώς σε λεπτές και εν συνεχεία σε υπέκλεπτες τομές της τάξης των 11 nm. Χρησιμοποιήθηκε υπερμικροτόμος τύπου Reichert.
Τα παρασκευάσματα εχρώσθησαν με οξικό ουρανύλιο, και κιτρικό μόλυβδο, εξετάσθηκαν σε ηλεκτρονικό μικροσκόπιο τύπου Zeiss 9 aS υπό τάση 80 KV και φωτογραφήθηκαν.
Αποτελέσματα
Α) Τα αστροκυττώματα εμφανίζουν ορατές αστροκυτταρικές προσεκβολές-ορατές και υπό το οπτικό μικροσκόπιο- οι οποίες διατάσσονται περιαγγειακώς και σχηματίζουν μεταξύ τους πυκνό πλέγμα.
Β) Τόσο εντός των κυττάρων όσο και εντός των προσεκβολών παρατηρούνται πολυάριθμες νευρογλοιακές ίνες που σχηματίζουν πυκνές δέσμες και αποτελούν το παθογνωμονικό κριτήριο των αστροκυττωμάτων (Εικ. 1).
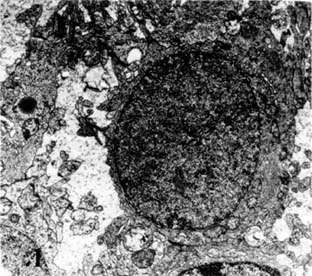
Γ) Πολυάριθμα μιτοχόνδρια που σχηματίζουν σφαιροειδείς ομάδες.
Δ) Εντός του κυτταρικού σώματος παρατηρείται εν εκτάσει κατάσπαση του λείου ενδοπλασματικού δικτύου και της συσκευής του Golgi.
Ε) Τα νεοπλασματικά κύτταρα παρουσιάζουν κατάτμηση των μικροσωληναρίων ενώ τα διάμεσα ινίδια εναποτίθενται σε παράλληλες δέσμες. Φέρουν δε σπανίως πινοκυτταρικά κυστίδια στην ελεύθερη επιφάνειά τους. (Εικ. 2, 3).
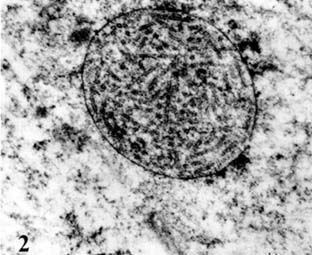
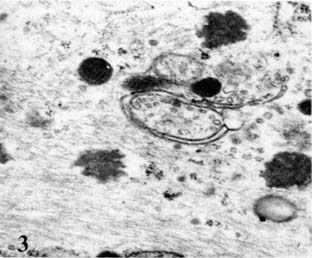
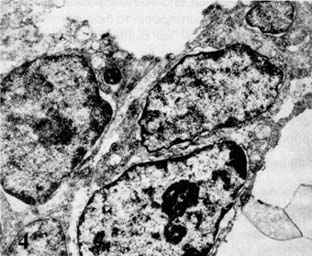
ΣΤ) Ο πυρήνας των κυττάρων παρουσιάζει αδρά κατανομή της χρωματίνης. Αυτή φέρεται ως ετεροχρωματίνη και κατανέμεται τόσο στην περιφέρεια του πυρήνα όσο και εντός της κεντρικής μοίρας αυτού και των δακτυλιοειδών προσεκβολών των πυρήνων. (Εικ. 4).
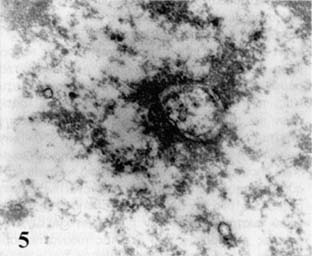
Ζ) Όχι σπάνια παρατηρούνται εκκολπωματώδεις προσεκβολές του κυτταροπλάσματος εντός του πυρήνα. Σε αυτές τις ενδοπυρηνικές εκκολπώσεις είναι εμφανής η διεύρυνση του λείου ενδοπλασματικού δίκτύου και της συσκευής Golgi καθώς και δέσμες νευρογλοιακών ινών (Εικ. 5).
Συζήτηση
Η ταξινόμηση των αστροκυττωμάτων επί μακρόν αποτελούσε αντικείμενο αντιπαράθεσης στον επιστημονικό χώρο, γεγονός που αντικατοπτρίζεται στην ύπαρξη, πολλών ταξινομικών συστημάτων χωρίς κανένα από αυτά να έχει γίνει καθολικά αποδεκτό.
Ο Kernohan εισήγαγε την αριθμητική ταξινόμηση σε βαθμούς από το Ι ως το V ακολουθώντας το σύστημα ταξινόμησης των καρκινωμάτων του Broders. Βασίσθηκε στην παρουσία ορισμένων χαρακτήρων όπως ο αριθμός των μιτώσεων, ο πυρηνικός πλειομορφισμός, η ατυπία και όσον αφορά στην πρόγνωση ξεχώριζε δύο διαφορετικές ομάδες, την ομάδα αστροκυττωμάτων βαθμού Ι & IΙ και την ομάδα αστροκυττωμάτων βαθμού ΙΙΙ & IV.1
Ο Ringertz εισήγαγε το σύστημα τριών βαθμών χρησιμοποιώντας τους όρους «αστροκύττωμα», «αστροκύττωμα ενδιάμεσου τύπου» και «γλοιοβλάστωμα» εξετάζοντας τον πλειομορφισμό, την κυτταροβρίθεια, τις μιτώσεις, την νεοαγγείωση και τις νεκρώσεις20.
Το σύστημα WH021 ταξινομεί τους όγκους ως «αστροκύττωμα», «αναπλαστικό αστροκύττωμα» και «πολύμορφο γλοιοβλάστωμα» βασιζόμενο στον εντοπισμό τεσσάρων κυρίως ιστοπαθολογικών κριτηρίων: της κυτταροβρίθειας, του πλειομορφισμού, στην ύπαρξη νεοαγγείωσης και νεκρώσεων.
Πρέπει να επισημανθεί η μεγάλη συμβολή των Rusell και Rubinstein οι οποίοι στις μελέτες τους επάνω στην ιστοπαθολογική ταξινόμηση των όγκων του ΚΝΣ αποδίδουν ιδιαίτερη βαρύτητα στον εντοπισμό στοιχείων κακοήθειας με τη μορφή ψευδοπασσαλιδωτής διάταξης των κυττάρων22.
Η Daumas - Duport23 προτείνει μια απλή ταξινόμηση βασιζόμενη στην παρουσία ή απουσία τεσσάρων μορφολογικών κριτηρίων της πυρηνικής ατυπίας, των μιτώσεων, των ενδοθηλιακών εκβλαστήσεων και των νεκρώσεων. Ταξινομεί τα αστροκυττώματα σε τέσσερεις ομάδες από 1-4 όπου 0 κριτήρια=Gradel, 1 κριτήριο=Grade 2,2 κριτήρια=Grade 3 και όπου εντοπίζονται 3 ή 4 κριτήρια = Grade 4. Το σύστημα της Daumas - Duport φαίνεται πως εξυπηρετεί καλύτερα την ανάγκη συσχέτισης ενός ταξινομικού συστήματος με την πρόγνωση και τυγχάνει ευρείας εφαρμογής3,20,24, έχοντας πιθανά περιορισμό στη χρήση στους ενήλικες καθώς δεν συσχετίζεται ικανοποιητικά με την πρόγνωση όταν εφαρμόζεται στον παιδιατρικό πληθυσμό ασθενών25.
Τα περισσότερα ταξινομικά συστήματα έχουν ορισμένα μειονεκτήματα διότι
α) τα ιστολογικά κριτήρια είναι υποκειμενικά και
β) οι παθολογοανατόμοι δεν χρησιμοποιούν κοινά και ταυτοποιημένα κριτήρια για την ταξινόμηση των όγκων αυτών γι' αυτό και η αξιολόγησή τους πολλές φορές διαφέρει ανάλογα με το εργαστήριο.
Για τους λόγους αυτούς πολλές φορές συναντάμε αλληλοκαλυπτόμενους όρους όπως «αστροκύττωμα Ι προς ΙΙ» ή «αστροκύττωμα ΙΙ προς ΙΙΙ»20, οι οποίοι συχνά προκαλούν σύγχυση ή και αμηχανία όσον αφορά στη θεραπευτική προσέγγιση.
Τα διαγνωστικά διλήμματα στη βιοψία ιστοπαθολογικού υλικού δεν είναι σπάνια και συχνά είναι το αποτέλεσμα πολλών παραγόντων οι οποίοι περιλαμβάνουν
α) τα artifacts καθήλωσης (fixation artifacts).
β) το μέγεθος του ιστοτεμαχίου που λαμβάνεται για παθολογοανατομική εξέταση.
γ) την αποτυχία των ανοσοϊστοχημικών μεθόδων να ξεχωρίσουν διάφορους κυτταρικούς τύπους και
δ) την άγνοια ορισμένων σπανίων μορφών26.
Η ορθή διάγνωση και η επιβεβαίωση της διάγνωσης είναι απαραίτητες και σε ορισμένες περιπτώσεις απαιτούν και την εξέταση υπό το ηλεκτρονικό μικροσκόπιο. Ενίοτε η χρήση του ηλεκτρονικού μικροσκοπίου μπορεί να είναι η μόνη μέθοδος που θα οδηγήσει σε ασφαλή διάγνωση αναγνωρίζοντας τους αναπλαστικούς
χαρακτήρες του όγκου. Παρά το γεγονός ότι πρόκειται για μία εξειδικευμένη και πολυέξοδη εξέταση, που πολύ απέχει ώστε να συμπεριληφθεί στις εξετάσεις «ρουτίνας», μπορεί να καταστεί πολύτιμη όπου και όταν υπάρχει δυσχέρεια στην διάγνωση όπως για παράδειγμα όταν το αποστελλόμενο υλικό βιοψίας είναι πολύ μικρό για να τεθεί ασφαλής ιστοπαθολογική και ανοσοϊστοχημική διάγνωση. Υπάρχουν περιπτώσεις επίσης όπου ασαφής ιστοπαθολογική διάγνωση προκαλεί αμηχανία ως πρός την θεραπευτική προσέγγιση όπως για παράδειγμα να διακινδυνεύσει ή όχι ο θεράπων ιατρός την ιατρογενή ανάπτυξη μετακτινικών νεκρώσεων σε ένα νέο άτομο με νεοπλασία που χαρακτηρίστηκε «αστροκύττωμα Ι πρός ΙΙ» στέλνοντάς το για ακτινοθεραπεία.
Πιστεύουμε πως σε δύσκολες διαγνωστικά περιπτώσεις η εξέταση υπό το ηλεκτρονικό μικροσκόπιο έρχεται να συμπληρώσει το διαγνωστικό φάσμα των ιστοπαθολογικών και ανοσοιστοχημικών κριτηρίων. Με τις σύγχρονες δε και ταχείες μεθόδους παρασκευής και μελέτης του υλικού μέσα σε λίγες ώρες μετά την παραλαβή του από τον χώρο του χειρουργείου καθίσταται δυνατή πολλές φορές η προσέγγιση της οριστικής διαγνώσεως πριν την συμπλήρωση του χειρουργικού χρόνου.
ΒΙΒΛΙΟΓΡΑΦΙΑ