| |||
| |||
Τεχνητή νοημοσύνη και νόσος του Alzheimer
ΠΑΡ. ΧΑΜΛΑΤΖΗΣ*, ΣΜΟΛΩΦ-ΑΛΕΞ. ΧΑΜΛΑΤΖΗΣ**
*Αναπληρωτής Καθηγητής, Α' Νευρολογική Κλινική ΑΠΘ, Νοσοκομείο ΑΧΕΠΑ, Θεσσαλονίκη
**Προγραμματιστής-Αναλυτής
Περίληψη
Σύμφωνα με διάφορες μελέτες το 33% του συνόλου των ανοϊκών καταστάσεων οφείλεται
σε κάποια ανατάξιμη διαταραχή (υποθυρεοειδισμό, ανεπάρκεια βιταμίνης Β12, κτλ)
ενώ το υπόλοιπο 67% σε κάποια νευροεκφυλιστική πάθηση. Το 90% των θυμάτων της
δεύτερης αυτής ομάδας πάσχει από τη νόσο του Alzheimer. Δεδομένου του γεγονότος
ότι οι όποιες θεραπευτικές παρεμβάσεις έχουν πιθανότητα επιβράδυνσης της εξέλιξης
της πάθησης αυτής μόνο στις ελαφράς και μέτριας βαρύτητας περιπτώσεις, ιδιαίτερη
σημασία αποκτά η έγκαιρη διάγνωση. Στα πλαίσια αυτά σημαντική φαίνεται ότι είναι
η συμβολή της τεχνητής νοημοσύνης με τη μορφή των τεχνητών νευρωνικών δικτύων.
Βάσει ενός αριθμού αξιόλογων μελετών προκύπτει ότι τα τεχνητά νευρωνικά δίκτυα προσφέρουν μεγάλες δυνατότητες για τη βελτίωση της διαγνωστικής ακρίβειας εκείνων των δοκιμασιών που εμφανίζουν σύνθετα πρότυπα δεδομένων, όπως τομογραφίες εκπομπής ποζιτρονίων (PET), μονήρους εκπομπής φωτωνίων (SPECT), κτλ, τα οποία δύσκολα τα διακρίνει ακόμη και ο εξειδικευμένος παρατηρητής. Η ικανότητά τους να ανιχνεύουν ανώτερης τάξης μη γραμμικές σχέσεις μεταξύ των δεδομένων που επεξεργάζονται (τα οποία χρησιμεύουν ως δείκτες διαφοροποίησης των παθολογικών περιστατικών), τα καθιστά ισχυρά ταξινομικά εργαλεία με επιδόσεις συγκρίσιμες προς αυτές των εξειδικευμένων επιστημόνων και σε πολλές περιπτώσεις ανώτερες των διαφόρων στατιστικών μεθόδων.
Λέξεις κλειδιά: Τεχνητή νοημοσύνη, νόσος του Alzheimer.
Eισαγωγή
Σύμφωνα με μία σχετικά πρόσφατη μελέτη1 το 33% του συνόλου των ανοϊκών καταστάσεων οφείλεται σε κάποια ανατάξιμη διαταραχή (υποθυρεοειδισμό, ανεπάρκεια βιταμίνης Β12, κτλ) ενώ το υπόλοιπο 67% σε κάποια νευροεκφυλιστική πάθηση. Το 90% των θυμάτων της δεύτερης αυτής ομάδας πάσχει από τη νόσο του Alzheimer. Το ανοϊκό σύνδρομο που χαρακτηρίζει την πάθηση αυτή είναι αποτέλεσμα νευρωνικού θανάτου που προηγείται κατά πολλά έτη της εγκατάστασης των διαταραχών της μνήμης και των άλλων συμπτωμάτων. Η βαθμιαία και αδιόρατη εγκατάσταση των συμπτωμάτων αυτών οφείλεται στη δυνατότητα των νευρικών κυττάρων να αντισταθμίζουν λειτουργικά το κυτταρικό έλειμμα διά των επιζώντων νευρώνων, ακόμη και στην περίπτωση που ο κυτταρικός πληθυσμός έχει ερημωθεί κατά τα 4/5 του αρχικού του αριθμού. Τα συμπτώματα της πάθησης θα αρχίσουν να εμφανίζονται όταν το εναπομείναν 1/5 των υγιών νευρώνων αρχίσει να μειώνεται δραματικά, οπότε πλέον και η κατάσταση καθίσταται μη αναστρέψιμη2. Ο επιπολασμός της πάθησης αυτής στο γενικό πληθυσμό κυμαίνεται στο 1-2%, ενώ στα άτομα άνω των 65 ετών ανέρχεται στο 5-10% και στα άτομα άνω των 80 ετών φθάνει στο 20-30%. Υπολογίζεται ότι σήμερα στις Ηνωμένες Πολιτείες της Αμερικής 4 εκατομμύρια άνθρωποι πάσχουν από τη νόσο αυτή και εκτιμάται ότι ο αριθμός αυτός θα ανέλθει στα 14 εκατομμύρια στο έτος 2040 άν μέχρι τότε δεν βρεθεί κάποιος αποτελεσματικός τρόπος πρόληψης ή θεραπείας της πάθησης αυτής. Με σημερινά δεδομένα το κόστος νοσηλείας και θεραπείας των ασθενών που πάσχουν από τη νόσο του Alzheimer, σε ό,τι αφορά τις Ηνωμένες Πολιτείες της Αμερικής τουλάχιστον, ανέρχεται στο ιλιγγιώδες ποσό των 100 δισεκατομμυρίων δολλαρίων ετησίως. Δεδομένου του γεγονότος ότι οι όποιες θεραπευτικές παρεμβάσεις έχουν πιθανότητα επιβράδυνσης της εξέλιξης της πάθησης μόνο στις ελαφράς και μέτριας βαρύτητας περιπτώσεις3, ιδιαίτερη σημασία αποκτά η έγκαιρη διάγνωση της πάθησης. Προς το παρόν, μόνο η βιοψία του εγκεφάλου και η ανεύρεση των χαρακτηριστικών ιστοπαθολογικών ανωμαλιών (νευροϊνιδιακές βλάβες, γεροντικές πλάκες) μπορεί να καλύψει το 100% της διάγνωσης. Παρά ταύτα η θέσπιση ειδικών διαγνωστικών κριτηρίων (ICD-10, DSM-IV, NINCDS-ADRDA) και η προσφερόμενη βοήθεια από τη σύγχρονη παρακλινική έρευνα, ανέβασε την ακρίβεια της διάγνωσης στο 80-90% περίπου των περιπτώσεων. Στα πλαίσια αυτά και μέχρις ότου βρεθεί η ιδανική ταχεία, απλή, ακριβής, φθηνή, μη παρεμβατική δοκιμασία, κάθε προσφορά στον τομέα της διάγνωσης είναι ευχαρίστως αποδεκτή. Μια τέτοια προσφορά φαίνεται ότι παρέχει η τεχνητή νοημοσύνη με τη μορφή των τεχνητών νευρωνικών δικτύων.
Τεχνητή νοημοσύνη
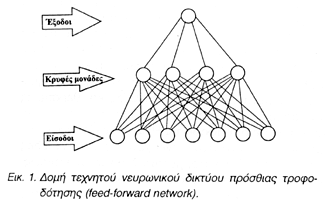
Η τεχνητή νοημοσύνη (artificial intelligence), ως ξεχωριστό πεδίο έρευνας, άρχισε να αναδύεται κατά τη 10ετία του 1940, όμως κύριο ορόσημό της θεωρείται η 10ετία του 1950 όταν οι ηλεκτρονικοί υπολογιστές άρχισαν να γίνονται μια εμπορική πραγματικότητα4. Η έρευνα πάνω στην τεχνητή νοημοσύνη βασίζεται, μεταξύ των άλλων τεχνικών, και στην επεξεργασία της πληροφορίας δια μέσου της νευρομίμησης, με τη χρήση των λεγόμενων τεχνητών νευρωνικών δικτύων (artificial neural networks). Στις βασικές ιδιότητες των τεχνητών νευρωνικών δικτύων ανήκουν η δυνατότητά τους για εκπαίδευση ώστε να αντιμετωπίζουν το απρόβλεπτο και η ικανότητά τους να διδάσκονται από την πείρα τους. Ως προς τα βασικά δομικά του στοιχεία, ένα τεχνητό νευρωνικό δίκτυο αποτελείται από τις μονάδες εισόδου, από τις ενδιάμεσες ή κρυφές μονάδες και από την ή τις μονάδες εξόδου5 (Εικ. 1). Οι μονάδες εισόδου αποτελούν το αντίστοιχο των νευρώνων, όπου γίνεται η παράλληλη επεξεργασία των δεδομένων που εισέρχονται στο δίκτυο. Οι ενδιάμεσες ή κρυφές μονάδες, είναι σε θέση να προσδιορίζουν ανώτερης τάξης μη γραμμικές ομοιότητες μεταξύ των δεδομένων που επεξεργάζεται το δίκτυο. Τέλος, στις μονάδες εξόδου θα εμφανισθεί η τελική απάντηση στο ερέθισμα που εφαρμόσθηκε στις μονάδες εισόδου. Οι διάφορες μονάδες είναι συνδεδεμένες μεταξύ τους με ζυγισμένες συνδέσεις (weighted connections), οι συντελεστές βαρών των οποίων δρούν ευωδοτικά ή ανασταλτικά στη μεταφορά της πληροφορίας σε άλλες μονάδες και αντιστοιχούν προς τις νευρικές συνάψεις.
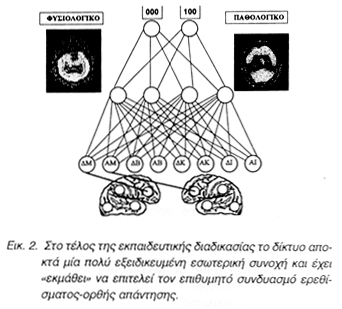
Η έννοια της μάθησης αποτελεί μία από τις πλέον χαρακτηριστικές ιδιότητες των τεχνητών νευρωνικών δικτύων. Κατά την εκπαίδευση υπό «επίβλεψη», ένας αριθμός προτύπων εκπαίδευσης παρουσιάζεται στις εισόδους του δικτύου, καθένα από τα οποία συνδυάζεται με μία γνωστή ορθή απάντηση. Αν μετά την επεξεργασία των δεδομένων, η απάντηση στην έξοδο του δικτύου δεν ταυτίζεται με την ορθή, το σφάλμα λαμβάνει μία τιμή και η διαδικασία επαναλαμβάνεται, μετά από τροποποίηση κάθε φορά των συνδέσεων του δικτύου. Η επεξεργασία των δεδομένων συνεχίζεται κατ΄ αυτό τον τρόπο (έως και μερικές χιλιάδες φορές σε κάποιες περιπτώσεις) μέχρις ότου το σφάλμα μηδενισθεί ή μειωθεί αισθητά και στην έξοδο του δικτύου ληφθεί η ορθή απάντηση. Στο τέλος της εκπαιδευτικής διαδικασίας το δίκτυο αποκτά μία πολύ εξειδικευμένη εσωτερική συνοχή και έχει «εκμάθει» να επιτελεί τον επιθυμητό συνδυασμό ερεθίσματος-ορθής απάντησης (Εικ. 2),. Τα δίκτυα αυτά πρόσθιας τροφοδότησης (feed-forward networks), όπως λέγονται, ουσιαστικά διδάσκονται από τα σφάλματά τους. Έτσι, μετά την κατάλληλη εκπαίδευση, το νευρωνικό δίκτυο είναι σε θέση, με τη βοήθεια μίας σχετικά περιορισμένης δεξαμενής πληροφοριών, να επιτελεί μία γενική λειτουργία. Επί παραδείγματι, από μία μικρή συλλογή εικόνων αυτοκινήτου να μπορεί τελικά να ξεχωρίζει το αυτοκίνητο από τα άλλα οχήματα. Έναν άλλο τύπο μάθησης αποτελεί η εκπαίδευση χωρίς «επίβλεψη». Στην περίπτωση αυτή δεν υπάρχει το επιθυμιτό τελικό αποτέλεσμα στην έξοδο του δικτύου αλλα η ταξινόμηση των προτύπων διδασκαλίας γίνεται σύμφωνα με τις κοινές ομοιότητές τους.
Βάσει των παραπάνω θα μπορούσε να πεί κανείς ότι η τεχνητή νοημοσύνη μιμείται τη βασική διεργασία μάθησης του ανθρωπίνου εγκεφάλου, όπου κάθε καινούρια γνώση ενσωματώνεται στις προϋπάρχουσες και καθίσταται προσιτή για μελλοντική χρήση. Πρόκειται δηλαδή για μία προσπάθεια εξομοίωσης της φυσικής νοημοσύνης σε ψηφιακούς υπολογιστές.
Τα λεγόμενα έμπειρα συστήματα (expert systems) είναι παράγωγα της τεχνητής νοημοσύνης και αποτελούν την εφαρμογή της στην καθημέρα πράξη. Σύμφωνα με τον ορισμό του Jackson6, το έμπειρο σύστημα είναι ένα πρόγραμμα ηλεκτρονικού υπολογιστή που αναπαριστά τη γνώση κάποιου ειδικού πάνω σε ένα αντικείμενο, και από την άποψη αυτή είναι σε θέση να επιλύει περίπλοκα προβλήματα ή να δίνει εξειδικευμένες συμβουλές.
Τα πεδία πρακτικών εφαρμογών των έμπειρων συστημάτων, είτε με την αρχιτεκτονική των τεχνητών νευρωνικών δικτύων είτε με άλλου τύπου αρχιτεκτονικές, είναι ευρύτατα και καταλαμβάνουν ένα μεγάλο φάσμα επιστημών που εκτείνεται από τη μηχανική, τη φυσική, τα μαθηματικά και την επιστήμη των ηλεκτρονικών υπολογιστών, μέχρι την ψυχολογία και τη νευροβιολογία.
Ειδικότερα, στον τομέα της ιατρικής5 το πρώτο έμπειρο σύστημα με το όνομα MYCIN αναπτύχθηκε από το Πανεπιστήμιο του Stanford στη 10ετία του 1960 και είχε ως σκοπό τον καθορισμό της διάγνωσης και την ενδεικνυόμενη θεραπεία σε περίπτωση λοιμώδους πάθησης. Το ποσοστό επιτυχίας του συστήματος αυτού σε μία από τις τελευταίες αξιολογήσεις του με περιπτώσεις μηνιγγίτιδος διαφόρου αιτιολογίας, έφθασε στο 70% και ήταν ανώτερο αυτού των ειδικών επιστημόνων που το συναγωνίσθηκαν.
Tεχνητή νοημοσύνη και νόσος του Alzheimer
Την τελευταία 10ετία είδαν το φως της δημοσιότητας ένας αριθμός αξιόλογων επιστημονικών εργασιών, που είχαν ως σκοπό την αξιολόγηση των δυνατοτήτων των τεχνητών νευρωνικών δικτύων στον τομέα της διάγνωσης της νόσου του Alzheimer. Στην πάθηση αυτή ένα σημαντικό ρόλο στη διαγνωστική αξιολόγηση των πασχόντων παίζει και η εγκεφαλική απεικόνιση με τη βοήθεια των σύγχρονων νευρο-απεικονιστικών μεθόδων (αξονική και μαγνητική τομογραφία). Όμως, η ποιοτική διαφοροποίηση των εικόνων αυτών ώστε να διαχωρίζονται οι πάσχοντες από τους υγιείς, κυρίως στα αρχικά στάδια της νόσου, είναι ένα ιδιαίτερα δυσχερές έργο. Έτσι, γνωστού όντος ότι οι διαταραχές του εγκεφαλικού μεταβολισμού στις περιπτώσεις αυτές προηγούνται χρονικά των δομικών μεταβολών του εγκεφάλου, ήταν επόμενο η απεικόνιση των μεταβολών αυτών να αποτελεί ένα πιο ευαίσθητο διαγνωστικό δείκτη της πάθησης.
Όμως, στη νόσο του Alzheimer δεν υπάρχει μία παθογνωμονική διαταραχή που να αφορά μόνο μία περιοχή του εγκεφάλου (π.χ τον κροταφικό ή τον βρεγματικό λοβό) και επομένως είμεθα ενώπιον ενός προβλήματος μη γραμμικού διαχωρισμού δεδομένων, που θα διαφοροποιήσουν τους πάσχοντες από τους υγιείς. Η δυνατότητα των τεχνητών νευρωνικών δικτύων να προσδιορίζουν ανώτερης τάξης μη γραμμικές ομοιότητες μεταξύ των δεδομένων, αποτέλεσε την πρόκληση ώστε να δοκιμασθούν σε ανάλογες ερευνητικές εργασίες.
Σε ένα αριθμό μελετών η κύρια συνεισφορά των τεχνητών νευρωνικών δικτύων συνίσταται στην αναγνώριση ανώμαλων μεταβολικών προτύπων (pattern) της διαγνωστικής απεικονιστικής. Στις μελέτες αυτές χρησιμοποιούνται συνήθως δεδομένα που προέρχονται από τομογραφίες εκπομπής ποζιτρονίων (PET) ή μονήρους εκπομπής φωτωνίων (SPECT).
Η έρευνα με τομογραφίες εκπομπής ποζιτρονίων απέδειξε την ύπαρξη «τυπικών» διαταραχών του μεταβολισμού της γλυκόζης (fluoro-deoxy-glucose PET scan) στον εγκέφαλο ατόμων με άνοια τύπου Alzheimer, σύμφωνα με τα διεθνώς αναγνωρισμένα κριτήρια NINCDS/ADRDA ή DSM-VI. Στις περιπτώσεις αυτές το πλέον χαρακτηριστικό εύρημα ήταν η μείωση του μεταβολισμού (συμμετρική ή ασύμμετρη) στις κροταφοβρεγματικές, κυρίως όμως στις μετωπιαίες περιοχές7, ώστε βάσει του στοιχείου αυτού, να διαχωρίζεται ευχερώς η ομάδα των πασχόντων από την ομάδα ελέγχου. Εν τούτοις, η αξιόπιστη ταξινόμηση ενός μεμονωμένου περιστατικού με βάση το ανώμαλο μεταβολικό του πρότυπο, παραμένει μία αρκετά δυσχερής υπόθεση, δεδομένου ότι και άλλα νοσήματα, όπως π.χ η παρκινσονική άνοια ή ο υδροκέφαλος φυσιολογικής τάσης, είναι δυνατό να εμφανίσουν το «τυπικό» παθολογικό πρότυπο της νόσου του Alzheimer. Ο μεγάλος αριθμός περιοχών του εγκεφάλου από όπου προέρχονται τα δεδομένα του ΡΕΤ, η εγγενής μεταβλητότητα των δεδομένων αυτών και τα ενδεχόμενα μεθοδολογικά σφάλματα συμβάλλουν έτι περαιτέρω στη σημαντική ποικιλομορφία μεταξύ των διαφόρων περιστατικών. Έτσι, συχνά χρησιμοποιούνται στατιστικές μέθοδοι ανάλυσης, όπως π.χ η διακριτική ανάλυση (Discriminant analysis) για τον προσδιορισμό εκείνων των περιοχών του εγκεφάλου που εμφανίζουν τις μεγαλύτερες μεταβολικές διαφορές μεταξύ τους, ώστε τελικά να αποτελέσουν και τον κύριο δείκτη διαφοροποίησης των παθολογικών περιστατικών.
Για το σκοπό αυτό, σε μία μελέτη8 αξιολογήθηκε η επίδοση ενός τεχνητού νευρωνικού δικτύου (μετά από κατάλληλη εκπαίδευση), ενός ειδικού επιστήμονα στην ανάγνωση του ΡΕΤ και μίας μεθόδου στατιστικής ανάλυσης (διακριτική ανάλυση) στο διαχωρισμό του παθολογικού δείγματος (πιθανή ν. Alzheimer 41 ασθενείς και δυνατή ν. Alzheimer 39 ασθενείς) από το φυσιολογικό δείγμα (50 άτομα). Η σύγκριση των τριών μεθόδων αξιολόγησης του υλικού έγινε με τη βοήθεια μίας μεθόδου ανάλυσης γνωστής ως ROC (Relative Operating Characteristics). Η μέθοδος αυτή αποτελεί ουσιαστικά την γραφική παράσταση της σχέσης μεταξύ της ευαισθησίας (sensitivity) και της ειδικότητας (specificity) μίας εργαστηριακής δοκιμασίας9, δηλαδή της σχέσης μεταξύ της αναλογίας των αληθώς θετικών και των ψευδώς θετικών απαντήσεων της δοκιμασίας αυτής. Η περιοχή κάτω από την καμπύλη ROC μετράει την επίδοση ενός διαγνωστικού συστήματος σε διάφορες θέσεις του κριτηρίου απόφασης, και είναι πλέον αντιπροσωπευτική της αποτελεσματικότητας του συστήματος (όσο μεγαλύτερη η περιοχή κάτω από την καμπύλη τόσο καλύτερη η διαγνωστική επίδοση). Στην ομάδα με διάγνωση «πιθανή Alzheimer» οι περιοχές κάτω απο την καμπύλη ROC ήταν 0.85 για το νευρωνικό δίκτυο και 0.89 για τον εμπειρογνώμονα, ενώ στην ομάδα της «δυνατής Alzheimer» οι περιοχές ήταν 0.81 τόσο για το δίκτυο όσο και για τον εμπειρογνώμονα. Η μέθοδος της διακριτικής ανάλυσης υπολειπόταν αισθητά και των δύο (0.80 και 0.74 αντίστοιχα).
Σε μία άλλη μελέτη10 με 77 περιπτώσεις «πιθανής νόσου Alzheimer» και 124 άτομα της ομάδας ελέγχου χρησιμοποιήθηκαν δεδομένα από ΡΕΤ-κάμερα χαμηλής (PETT V) και υψηλής ανάλυσης (Scanditronix). Η ταξινόμηση του υλικού βάσει των δεδομένων του Scanditronix ήταν αισθητά καλύτερη (περιοχή ROC = 0.95) από αυτή βάσει του ΡΕΤΤ V (περιοχή ROC = 0.87). Έτσι, στη περίπτωση που άτομα με ήπιες γνωσιακές διαταραχές είχαν, σύμφωνα με το θεώρημα του Bayes, πιθανότητα 50% ύπαρξης της νόσου, μετά την εξέταση με το Scanditronix και εφόσον κατετάσσοντο από το δίκτυο στην παθολογική ομάδα, η πιθανότητα αυτή ανερχόταν πλέον στο 90%.
Η τομογραφία μονήρους εκπομπής φωτωνίων (SPECT) αποτελεί, μία πλέον διαδεδομένη και λιγότερο δαπανηρή από το ΡΕΤ, μέθοδο ελέγχου της εγκεφαλικής διάχυσης μετά από ενδοφλέβια χορήγηση ουσίας (Hexamethyl-propylene amine oxime) σεσημασμένης με τεχνήτιο 99 (HMPAO-99Tc). Οι μετρήσεις της τοπικής πρόσληψης της ουσίας από τον ιστό είναι σε θέση να απεικονίσουν σύνθετα πρότυπα της εγκεφαλικής δραστηριότητας προσφέροντας σημαντική διαγνωστική βοήθεια.
Στη νόσο του Alzheimer ποσοτικές μετρήσεις της εγκεφαλικής διάχυσης απεκάλυψαν ευρήματα ανάλογα με αυτά του ΡΕΤ. Όμως η ακρίβεια της διάγνωσης με τη βοήθεια του SPECT ήταν ιδιαίτερα μεταβλητή και εκυμαίνετο από το 85% έως το 100% στις βαρύτερες περιπτώσεις, ενώ δεν υπερέβαινε το 25% στις περιπτώσεις με τις ελαφρές γνωσιακές διαταραχές11.
Στη μελέτη του Dawson και συν.12 περιελήφθησαν 97 ασθενείς με πιθανή νόσο του Alzheimer και 64 φυσιολογικά άτομα ως ομάδα ελέγχου. Αρχικά χρησιμοποιήθηκε η μέθοδος της πολλαπλής γραμμικής παλινδρόμησης, ώστε με βάση τον αριθμό των σπινθηρισμών από 14 διαφορετικές περιοχές του εγκεφάλου, να διαχωρισθεί η ομάδα των ασθενών από το φυσιολογικό δείγμα. Ο διαχωρισμός με την βοήθεια της στατιστικής μεθόδου ήταν απογοητευτικός, διότι δεν ξεπέρασε το 33.5%. Όταν όμως τα ίδια δεδομένα χρησιμοποιήθηκαν για την εκπαίδευση ενός νευρωνικού δικτύου, η επιτυχής διαφοροποίηση της παθολογικής ομάδος έφθασε το 95%.
Σε μία άλλη μελέτη13 έγινε προσπάθεια διαχωρισμού ασθενών με άνοια τύπου Alzheimer (20 ασθενείς) και αγγειακή άνοια (22 ασθενείς) από ηλικιωμένα φυσιολογικά άτομα (25 περιπτώσεις). Μετά την εκπαίδευση του δικτύου με βάση τα αντιπροσωπευτικά χαρακτηριστικά της μέσης πρόσληψης του ιστού, η επιτυχής ταξινόμηση των ανοϊκών ασθενών (αμφοτέρων των ομάδων) σε σχέση με τα φυσιολογικά άτομα ανήλθε στο 94% (63 από τα 67 περιστατικά), ενώ η ορθή διαφοροποίηση των ασθενών με άνοια τύπου Alzheimer από τους ασθενείς με αγγειακή άνοια ήταν 80% και 86% αντίστοιχα.
Σε μία άλλη, σχετικά πρόσφατη μελέτη14, εκτιμήθηκε η ικανότητα ενός τεχνητού νευρωνικού δικτύου ταξινόμησης ασθενών με πιθανή Alzheimer. Για το σκοπό αυτό χρησιμοποιήθηκαν δεδομένα που προέρχονταν από τέσσερις περιοχές ενδιαφέροντος (πρόσθια κροταφική-οπίσθια κροταφοβρεγματική, αμφοτερόπλευρα) του εγκεφάλου και εβασίζοντο σε εικόνες SPECT. Το πρώτο σκέλος της μελέτης αφορούσε το διαχωρισμό των ασθενών (29 περιπτώσεις με ελαφρές έως μέτριες ανοϊκές διαταραχές) από τους υγιείς (10 άτομα ελέγχου). Στο δεύτερο σκέλος της μελέτης έγινε προσπάθεια ταξινόμησης 15 πρόσθετων περιστατικών, με πολύ ελαφρές έως ελαφρές ανοϊκές διαταραχές, με τη βοήθεια του τεχνητού νευρωνικού δικτύου που είχε δημιουργηθεί στο πρώτο σκέλος της μελέτης. Τα αποτελέσματα της μελέτης αυτής συγκρίθηκαν με αυτά της διακριτικής ανάλυσης μετά από χρήση των ιδίων δεδομένων. Σύμφωνα με τα αποτελέσματα της παραπάνω έρευνας το νευρωνικό δίκτυο επέτυχε να διαχωρίσει πλήρως την παθολογική ομάδα από την ομάδα ελέγχου (περιοχή ROC 1.00 για το δίκτυο και 0.94 για την διακριτική ανάλυση). Ως προς την ταξινόμηση των νέων περιστατικών, η περιοχή ROC εκυμάνθη από 0.86 έως 1.00 για το δίκτυο και 0.99 για τη στατιστική μέθοδο.
Οι μετρήσεις των γνωσιακών λειτουργιών με τη χρήση των διαφόρων νευροψυχολογικών δοκιμασιών χρησιμοποιούνται ευρέως τόσο για των διαχωρισμό των πασχόντων από τη νόσο του Alzheimer από τα ηλικιωμένα φυσιολογικά άτομα όσο και για τον καθορισμό της βαρύτητας ενός ανοϊκού συνδρόμου. Για τον σκοπό αυτό, σε μία άλλη πρόσφατη μελέτη15, χρησιμοποιήθηκε ένα τεχνητό νευρωνικό δίκτυο το οποίο τροφοδοτήθηκε με τα αποτελέσματα των μετρήσεων 11 νευροψυχολογικών δοκιμασιών που ελέγχουν τη μνήμη, την προσοχή, το λόγο, την εκμάθηση, την κινητική και οπτικο-χωρική ικανότητα, κτλ. Το υλικό της μελέτης αποτελείτο απο 92 ασθενείς με διάγνωση «πιθανή νόσος Alzheimer» και 43 ηλικιωμένα άτομα της ομάδας ελέγχου. Η σύγκριση των αποτελεσμάτων έγινε με αυτά που προέκυψαν από τη χρήση της στατιστικής μεθόδου της διακριτικής ανάλυσης. Βάσει των αποτελεσμάτων αυτών, το νευρωνικό δίκτυο διαχώρισε ορθά το 91.1% των περιπτώσεων, ενώ η στατιστική μέθοδος το 71.9%. Επιπρόσθετα, ως προς την επιτυχή ταξινόμηση του υλικού, ανάλογα με τη βαρύτητα του ανοϊκού συνδρόμου, το τεχνητό νευρωνικό δίκτυο υπερείχε της διακριτικής ανάλυσης κατά 20%.
Επίσης με άριστα αποτελέσματα χρησιμοποιήθηκαν τα νευρωνικά δίκτυα για το διαχωρισμό φυσιολογικού και παθολογικού εγκεφαλικού ιστού με τη χρήση του υπέρυθρου φάσματος, σε περιπτώσεις εγκεφάλων ιστοπαθολογικά επιβεβαιωμένης νόσου του Alzheimer και εγκεφάλων της ομάδας ελέγχου16. Τα νευρωνικά δίκτυα διεχώρισαν το 100% της παθολογικής ομάδας ενώ η μέθοδος της διακριτικής ανάλυσης το 98%.
Σε μία πολύ πρόσφατη μελέτη17 ένα νευρωνικό δίκτυο, μετά από κατάλληλη εκπαίδευση με ηλεκτροεγκεφαλογραφικά δεδομένα προερχόμενα από βρεγματο-ινιακές καταγραφές από 3 άτομα με νόσο του Alzheimer και ισάρaιθμα άτομα της ομάδας ελέγχου, διεχώρισε ορθά τα 5 από τα 7 άτομα της παθολογικής ομάδας και το σύνολο των ατόμων της ομάδας ελέγχου (7 άτομα).
Συμπερασματικά, βάσει των παραπάνω μελετών τα τεχνητά νευρωνικά δίκτυα προσφέρουν μεγάλες δυνατότητες για τη βελτίωση της διαγνωστικής ακρίβειας εκείνων των δοκιμασιών που εμφανίζουν σύνθετα πρότυπα δεδομένων, τα οποία δύσκολα τα διακρίνει ακόμη και ο εξειδικευμένος παρατηρητής. Η ικανότητά τους να ανιχνεύουν ανώτερης τάξης μη γραμμικές σχέσεις μεταξύ των δεδομένων που επεξεργάζονται (τα οποία χρησιμεύουν ως δείκτες διαφοροποίησης των παθολογικών περιστατικών), τα καθιστά ισχυρά ταξινομικά εργαλεία με επιδόσεις συγκρίσιμες προς αυτές των εξειδικευμένων επιστημόνων και σε πολλές περιπτώσεις ανώτερες των διαφόρων στατιστικών μεθόδων.
Εφόσον επιλυθούν διάφορα τεχνικά θέματα που επηρεάζουν τις επιδόσεις τους (π.χ βέλτιστος αριθμός κρυφών μονάδων, αριθμός επαναλήψεων κατά την εκπαιδευτική διαδικασία, κ.ά), έχουν να προσφέρουν πολλά στο μέλλον στην πρώιμη διάγνωση της νόσου του Alzheimer, στη παρακολούθηση του ρυθμού εξέλιξης της παθολογικής διεργασίας, στη διαφοροποίηση παρόμοιων συνδρόμων άλλης αιτιολογίας, στην καλύτερη συγκρότηση των παθολογικών ομάδων που συμμετέχουν στα διάφορα θεραπευτικά πρωτόκολλα, κτλ.
ΒΙΒΛΙΟΓΡΑΦΙΑ