| |||
| |||
Ο ρόλος του αιματοεγκεφαλικού φραγμού
εις την παθογένειαν της πολλαπλής σκληρύνσεως
ΣΤΑΥΡΟΣ Ι. ΜΠΑΛΟΓΙΑΝΝΗΣ
Α' Νευρολογική Κλινική Αριστοτελείου Πανεπιστημίου Θεσσαλονίκης
Περίληψις
Η πολλαπλή σκλήρυνσις εθεωρείτο επί πολλά έτη ως αινιγματική νόσος, αγνώστου
αιτιοπαθογενετικού υποβάθρου. Τα τελευταία είκοσι έτη, δεδομένα προερχόμενα
εκ της πειραματικής ερεύνης, ήτοι εκ του προτύπου της πειραματικής αλλεργικής
εγκεφαλομυελίτιδος και εκ της υποτροπιαζούσης τοιαύτης, επέτρεψαν να διαλευκανθούν
πολλαί πτυχαί αναφερόμεναι εις τους παθογενετικούς μηχανισμούς και τα επί μέρους
στάδια αυτών. Κατεδείχθη ότι η νόσος αποτελεί συνεχή αυτοανοσοβιολογικήν αντίδρασιν,
κατά την οποίαν έν εκ των αρχικών μορφολογικών φαινομένων είναι η περιαγγειακή
κυτταρική αντίδρασις, υποδηλούσα διαταραχήν του αιματοεγκεφαλικού φραγμού και
έξοδον εμμόρφων στοιχείων, χυμοκινών και κυττοκινών εις τον νευροπιληματικόν
χώρον. Ο αιματοεγκεφαλικός φραγμός αποτελεί έν πλαστικόν και δυναμικόν σύστημα,
το οποίον διαδραματίζει υπό φυσιολογικάς συνθήκας σημαντικόν ρόλον εις την διατήρησιν
της ομοιοστάσεως εις τον χώρον του κεντρικού νευρικού συστήματος. Τόσον αι κλεισταί
συνάψεις μεταξύ των ενδοθηλιακών κυττάρων και η βασική μεμβράνη επί της οποίας
επικάθηνται ταύτα, όσον και αι δομικαί και διαμεμβρανικαί πρωτεΐναι, αι οποίαι
πληρούν τον χώρον μεταξύ των κυτταρικών επιφανειών εις τας κλειστάς συνάψεις,
συγκροτούν έν ουσιώδες δομικόν και λειτουργικόν υπόβαθρον, το οποίον ελέγχει
και ρυθμίζει την διέλευσιν μοριακών παραγόντων εκ του αγγειακού αυλού προς τον
νευροπιληματικόν χώρον, διά της αναπτύξεως πολλών επί μέρους μηχανισμών προσλήψεως
και περαιτέρω προωθήσεως αυτών. Η δίοδος ενεργοποιημένων λεμφοκυττάρων εκ των
κλειστών συνάψεων κατά τα αρχικά στάδια της πολλαπλής σκληρύνσεως αποτελεί πολυδιάστατον
διεργασίαν, το αρχικόν στάδιον της οποίας συνίσταται εις την αλληλοεπίδρασιν
μορίων προσφύσεως μεταξύ των ενδοθηλιακών κυττάρων των τριχοειδών και των ενεργοποιημένων
λεμφοκυττάρων. Εις επόμενον στάδιον τα λεμφοκύτταρα διέρχονται της βασικής μεμβράνης
τη βοηθεία των ιντεγρινών και των μεταλλοπρωτεασών, επερχομένης ούτω της πλήρους
ρήξεως του αιματοεγκεφαλικού φραγμού, η οποία έχει ως εύλογον αποτέλεσμα την
ελευθέραν δίοδον τόσον αυτών όσον και των φλεγμονωδών πρωτεϊνών και την υπ'αυτών
προσβολήν του ελύτρου της μυελίνης, το οποίον περιβάλλει τους νευράξονας. Η
έγκαιρος αποκατάστασις του αιματο-εγκεφαλικού φραγμού είναι ουσιώδους σημασίας
διά την αντιμετώπισιν της πολλαπλής σκληρύνσεως. Η χορήγησις στεροειδών και
ιντερφερόνης β συμβάλλουν εις την αποκατάστασιν της ακεραιότητος των κλειστών
συνάψεων και κατ'επέκτασιν ασκούν ευεργετικήν επίδρασιν κατά τα αρχικά στάδια
της νόσου. Επιπροσθέτως παράγοντες αντιρροπούντες την οξειδωτικήν καταπόνησιν,
ανταγωνισταί των σερινικών πρωτεασών, ανταγωνισταί των υποδοχέων των διεγειρόντων
αμινοξέων, φλαβινοειδή, ως είναι αι ανθοκυανοσίδαι και τα προκυανιδολικά ολιγομερή,
οι ανταγωνισταί της φωσφοδιεστεράσης τύπου IV, ιδίως δε οι νευροτρόφοι παράγοντες,
ως είναι ο BDNF, δύνανται να ασκήσουν ευεργετικόν ρόλον διά της αποκαταστάσεως
και σταθεροποιήσεως του αιματοεγκεφαλικού φραγμού και της αποτροπής της περαιτέρω
εκθέσεως του περιαγγειακού χώρου εις τους κυτταρικούς και μοριακούς φλεγμονώδεις
παράγοντας.
Λέξεις κλειδιά: Αιματοεγκεφαλικός φραγμός, πολλαπλή σκλήρυνσις, ηλεκτρονική μικροσκόπησις.
Εισαγωγή
Η αιτιοπαθογένεια της πολλαπλής σκληρύνσεως αποτελεί σύνθετον και πολυσχιδές θέμα, εις το οποίον υπεισέρχονται πολυάριθμοι αυτόχθονοι παράγοντες και επιγενείς συντελεσταί, με αποτέλεσμα επί πολλά έτη να παραμένη ασαφές και σκοτεινόν το όλον πεδίον και μόλις κατά τα τελευταία έτη αρχίζει τούτο να διαυγάζη και να διακρίνωνται αι βασικαί οδοί, αι οποίαι ακολουθούμεναι θα ηδύναντο να προσεγγίσουν το περίγραμμα των κυριωτέρων παθογενετικών μηχανισμών.
Σήμερον όλον και περισσότερον καθίσταται αποδεκτόν, μετά από ενδελεχή μελέτην της πειραματικής αλλεργικής εγκεφαλομυελίτιδος και ιδίως της υποτροπιαζούσης τοιαύτης, ότι η όλη διεργασία της πολλαπλής σκληρύνσεως αποτελεί συνεχή ανοσοβιολογικήν αντίδρασιν1,2 προς το έλυτρον της μυελίνης και τας κυτταρικάς δομάς, αι οποίαι συνδέονται μετά του σχηματισμού αυτής.
Η όλη νόσος άρχεται διά οξείας ανοσοβιολογικής αντιδράσεως, η οποία συνεχώς πυροδοτουμένη και αναζωπυρουμένη μεταπίπτει εις την χρονιότητα, διενεργουμένη συνεχώς υπό άλλοτε άλλην έκτασιν, θίγουσα κατά κύριον λόγον το έλυτρον της μυελίνης και προκαλούσα ουσιώδεις αλλοιώσεις εις τον νευράξονα3.
Πολυάριθμοι αντιγονικώς δρώντες παράγοντες, συνδεόμενοι ως διαπιστούται μετά του συστήματος μείζονος ιστοσυμβατότητος τύπου ΙΙ4 ή μετά του γονιδίου της οστεοποντίνης5, συμμετέχουν εις το ευρύ πεδίον της πυροδοτήσεως των ανοσοβιολογικών αντιδράσεων και της κινητοποιήσεως κυτταρικών σχηματισμών τόσον εντός του κεντρικού νευρικού συστήματος όσον και εις τον ευρύτερον χώρον του οργανισμού. Μεταξύ των αντιγονικώς δρώντων παραγόντων η βασική πρωτεΐνη της μυελίνης, η πρωτεολιπιδική πρωτεΐνη και η γλυκοπρωτεΐνη η συνδεδεμένη μετά της μυελίνης φαίνεται ότι ασκούν καθοριστικόν ρόλον εις την έναρξιν και την κινητοποίησιν της ανοσοβιολογικής αντιδράσεως6.
Η σύνθεσις των αντισωμάτων, τόσον ως προς την φύσιν αυτών όσον και ως προς τον ρυθμόν και την διάρκειαν της παραγωγής των, εξατομικεύεται από ατόμου εις άτομον7.
Αι κυττοκίναι7 και ιδίως η ιντερλευκίνη-68 διαδραματίζουν ουσιώδη ρόλον εις την κυτταρικήν κινητοποίησιν των λεμφοκυττάρων και των νευρογλοιακών κυττάρων9 και ασκούν άλλοτε άλλης εκτάσεως κινητοποίησιν ή καταστολήν επί των νευρογλοιακών κυττάρων του Hortega και των μακροφάγων10.
Το στάδιον της ενάρξεως της νόσου, το οποίον είναι ιδιαιτέρως δυσχερές εις την προσπέλασιν, καθορίζεται τόσον από την πλειάδα των εξωγενών και εν πολλοίς περιβαλλοντολογικών παραγόντων όσον και από το γενετικόν υπόβαθρον του πάσχοντος ατόμου11, ως τούτο κατεδείχθη και επί των πειραματικών προτύπων των απομυελινωτικών διεργασιών11. Κατά το στάδιον αυτό το ουσιωδέστερον γεγονός είναι η διέλευσις των λεμφοκυττάρων διά μέσου του τοιχώματος των τριχοειδών και των μετατριχοειδών φλεβιδίων του κεντρικού νευρικού συστήματος και η εγκατάστασις αυτών εις τον περιαγγειακόν χώρον12 και ενίοτε διαχύτως εντός του νευροπιληματικού χώρου. Το γεγονός τούτο θέτει ευλόγως την ερώτησιν του ρόλου τον οποίον ενδεχομένως διαδραματίζει ο αιματοεγκεφαλικός φραγμός αφ'ενός μεν εις τα αρχικά στάδια, αφ' ετέρου δε εις την όλην πορείαν της πολλαπλής σκληρύνσεως.
Ο αιματοεγκεφαλικός φραγμός
Ο αιματοεγκεφαλικός φραγμός, περιγραφείς προ εκατόν και πλέον ετών υπό του Paul Ehrlich13, αποτελεί το ουσιωδέστερον προστατευτικόν σύστημα του εγκεφάλου από την ανεξέλεγκτον είσοδον ουσιών και παραγόντων, οι οποίοι θα ηδύναντο να αλλοιώσουν την εσωτερικήν αρμονίαν του κεντρικού νευρικού συστήματος και πολλάκις να δράσουν βλαπτικώς.
Το ανατομικόν υπόβαθρον του αιματοεγκεφαλικού φραγμού (Εικ.1) συνίσταται εις την ανάπτυξιν κλειστών συνάψεων μεταξύ των ενδοθηλιακών κυττάρων14, το εύρος των οποίων ανέρχεται μόλις εις 6nm, μη επιτρέπον την είσοδον εμμόρφων στοιχείων και παραγόντων εκ του πλάσματος, γεγονός το οποίον ανατρέπεται επί ρήξεως αυτού15.
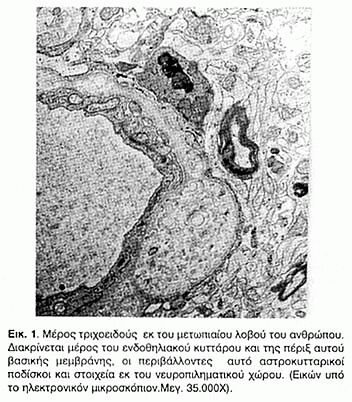
Πρωτεϊνικά στοιχεία, τα οποία αναπτύσσονται εντός των κλειστών συνάψεων είναι αρχικώς μεν η πρωτεΐνη ΖΟ-1, έχουσα μοριακόν βάρος 220 kDa και αποτελούσα μέρος των MAGUK πρωτεϊνών (γουανυλικαί κινάσαι συνδεόμεναι μετά των μεμβρανών), χρησιμεύουσα κυρίως διά την ανταλλαγήν πληροφοριών μεταξύ των κυττάρων, παραλλήλως προς την οποίαν αναπτύσσεται και η πρωτεΐνη ZO-2, έχουσα μοριακόν βάρος 160 kDa. Εις το σημείον της αμέσου επαφής των ενδοθηλιακών κυττάρων αναπτύσσονται αι καδχερίναι (E, P και Ν), αι οποίαι είναι διαμεμβρανικαί πρωτεΐναι αλληλοεπιδρώσαι, τη παρουσία ασβεστίου. Εν μέσω αυτών η VE-καδχερίνη ή καδχερίνη-5 φαίνεται ότι διαδραματίζει σημαντικόν ρόλον, ως μόριον διακυτταρικής συνδέσεως. Αι καδχερίναι συνδέονται εκ παραλλήλου μετά των κατενινών (α,β και γ), διά των οποίων συνδέονται μετ' εκείνων των στοιχείων του κυτταροσκελετικού συστήματος, τα οποία συνίστανται εξ ακτίνης.
Αι ουσιώδους βαρύτητος πρωτεΐναι, αι οποίαι αποφράσσουν στεγανώς τας κλειστάς συνάψεις περιλαμβάνουν τας οκλουδίνας, αι οποίαι είναι διαμεμβρανικαί και δομικαί πρωτεΐναι, τας κλαυδίνας και τας υπομεμβρανικάς πρωτεΐνας, τας αποφραττούσας την ζώνην προσφύσεως των ενδοθηλιακών κυττάρων, αι οποίαι είναι εκ των σημαντικοτέρων παραγόντων διαμορφώσεως της κλειστής συνάψεως, συνδεόμεναι μετά της ακτίνης και των σχηματισμών του κυτταροσκελετικού συστήματος.
Η όλη ανάπτυξις του αιματοεγκεφαλικού φραγμού ακολουθεί δύο επί μέρους στάδια ήτοι (α) το στάδιον της εμφανίσεως των οκλουδινών εις τον χώρον των κλειστών συνάψεων και (β) το στάδιον της καταλλήλου φωσφορυλιώσεως αυτών, η οποία πραγματοποιείται τη συμβολή αμφοτέρων των προσκειμένων ενδοθηλιακών κυττάρων16.
Επί της διεργασίας της φωσφορυλιώσεως των πρωτεϊνικών συστημάτων της κλειστής συνάψεως, ιδιαιτέραν σημασίαν έχει η φωσφορυλίωσις του μορίου της τυροσίνης, της β-κατενίνης, δι' ό και η συγκέντρωσις της τυροσινικής κινάσης είναι ιδιαιτέρως ηυξημένη εις τας μεμβρανικάς επιφανείας των κυττάρων, τα οποία θα συμβάλουν εις τον σχηματισμόν της κλειστής συνάψεως, ελαττουμένη μετά την πλήρη ωρίμανσιν αυτής.
Ο αναπτυσσόμενος ούτως ανατομικός φραγμός λειτουργικώς αντιρροπείται εν μέρει (α) εκ της πινοκυτταρικής δραστηριότητος των ενδοθηλιακών κυττάρων, (β) εκ της λειτουργίας συστημάτων υποβοηθουμένης ή ενεργητικής μεταφοράς, τα οποία δύνανται εκλεκτικώς να προσλάβουν τους απαιτουμένους παράγοντας και να προωθήσουν αυτούς μετά από διάλογον μεταξύ των ενδοθηλιακών κυττάρων και των περιβαλλόντων το τριχοειδές αστροκυττάρων17.
Αι προσλαμβανόμεναι ουσίαι διέρχονται από την βασικήν μεμβράνην του τριχοειδούς, το πάχος της οποίας ανέρχεται εις 30 nm, συνισταμένην εκ πρωτεϊνών, μεταξύ των οποίων ιδιαιτέραν σημασίαν έχουν η λαμινίνη και η ινονεκτίνη και φέρεται εις τους αστροκυτταρικούς ποδίσκους, οι οποίοι άπτονται του τοιχώματος των τριχοειδών, διατιθέμενοι κατά κανόνα εις πυκνάς σειράς, της αποστάσεως μεταξύ αυτών ανερχομένης εις 10-11 nm. Τα αστροκύτταρα φαίνεται εκ παραλλήλου, ότι εκτός του σχηματισμού της σειράς των αστροκυτταρικών ποδίσκων διαδραματίζουν σημαντικόν ρόλον εις την ανάπτυξιν και ωρίμανσιν των κλειστών συνάψεων μεταξύ των ενδοθηλιακών κυττάρων των τριχοειδών του εγκεφάλου, δεδομένου ότι η παρουσία αυτών αυξάνει τα επίπεδα του κυκλικού AMP.
Η πυκνή κατανομή των τριχοειδών εντός του κεντρικού νευρικού συστήματος εξασφαλίζει την ταχείαν παροχήν των απαιτουμένων παραγόντων εις τα νευρικά κύτταρα, εις σημείον ώστε η επιβίωσις αυτών να διασφαλίζεται σταθερώς εις οιανδήποτε θέσιν του εγκεφάλου, της παρεγκεφαλίδος ή του νωτιαίου μυελού. Θεωρείται, ότι εντός δύο δευτερολέπτων, ο νευρών δύναται να προσλάβη τα απαιτούμενα μόρια γλυκόζης εις όλας τας περιοχάς του κεντρικού νευρικού συστήματος διά μέσου ενός δικτύου τριχοειδών, τα οποία εν αναλύσει καταλαμβάνουν εν τω συνόλω των επιφάνειαν, ανερχομένην εις 12.000-18.000 τετραγωνικά εκατοστά.
Μηχανισμοί διόδου παραγόντων διά του αιματοεγκεφαλικού φραγμού
Η δίοδος διά των ενδοθηλιακών κυττάρων των τριχοειδών του κεντρικού νευρικού συστήματος διαφοροποιείται αναλόγως της δομής και των φυσικοχημικών ιδιοτήτων των διερχομένων ουσιών18.
Ούτω λιποδιαλυταί και μη ηλεκτρικώς πεφορτισμέναι ουσίαι, ως είναι τα οπιοειδή, η αλκοόλη και αι ξανθίναι διέρχονται παθητικώς, διαλυόμεναι εντός του λιποειδικού παράγοντος των μεμβρανικών συστημάτων, ενώ πολλαί εξ αυτών εισέρχονται εις τα ενδοθηλιακά κύτταρα διά πινοκυτταρώσεως.
Ηλεκτρικώς πεφορτισμέναι ουσίαι, ως είναι τα αμινοξέα, αι αμίναι, η γλυκόζη και τα νουκλεοτίδια διέρχονται τη βοηθεία συστημάτων μεταφορέων. Ετεραι ουσίαι εισέρχονται διά μέσου συστήματος υποδοχέων ή αντλιών εισόδου.
Φαρμακολογικοί παράγοντες ως είναι η L-dopa, η γκαμπαπεντίνη, η μπακλοφαίνη και έτεραι ανάλογοι ως προς την μοριακήν δομήν ουσίαι εισέρχονται εντός των ενδοθηλιακών κυττάρων χρησιμοποιούσαι τα συστήματα μεταφοράς των αρωματικών αμινοξέων19.
Παραλλήλως προς την είσοδον ουσιών διά των ενδοθηλιακών κυττάρων παρατηρείται και έξοδος εξ αυτών. Είς εκ των σημαντικοτέρων μηχανισμών εξωκυτταρώσεως είναι ο πραγματοποιούμενος τη βοηθεία της γλυκοπρωτεΐνης P, η οποία είναι διαμεμβρανική πρωτεΐνη, αναπτύσσουσα 12 διαμεμβρανικά πεδία και τρείς θέσεις γλυκοζυλιώσεως, αι οποίαι ευρίσκονται επί μίας εκ των εξωτερικών αγκυλών του μορίου αυτής.
Η γνώσις του τρόπου διόδου των διαφόρων ουσιών διά μέσου των ενδοθηλιακών κυττάρων και του αιματοεγκεφαλικού φραγμού καθίσταται ιδιαιτέρως πολύτιμος τόσον διά την κατανόησιν των ανοσοβιολογικών διεργασιών του κεντρικού νευρικού συστήματος όσον και διά τον σχεδιασμόν νέων φαρμακολογικών παραγόντων, οι οποίοι θα ηδύναντο να συμβάλλουν ευεργετικώς εις την ρύθμισιν των διεργασιών του εγκεφάλου επί νευρολογικών και ψυχιατρικών παθήσεων19.
Η όλη όμως λειτουργικότης του αιματοεγκεφαλικού φραγμού δεν είναι πάντοτε σταθερά, υποκειμένη εις πολλάς τροποποιήσεις συναρτήσει της ηλικίας του ατόμου20 και της επιδράσεως τοξικών παραγόντων, της λειτουργικότητος των ζωτικών οργάνων και της νοητικής στάθμης του πάσχοντος, επί ατόμων προβεβηκυίας ηλικίας21. Εκ παραλλήλου η μελέτη της κλειστής συνάψεως και των πρωτεϊνών, αι οποίαι συμβάλλουν εις την στεγανοποίησιν αυτής έχει υψίστην σημασίαν διά την αντιμετώπισιν νευρολογικών παθήσεων, η έναρξις των οποίων συνδέεται μετά της ρήξεως του αιματοεγκεφαλικού φραγμού ή μετά της ανεπαρκείας της λειτουργικότητος της κλειστής συνάψεως22.
Είναι γνωστόν ότι πολλοί παράγοντες φαρμακολογικοί ή ετέρας φύσεως δύνανται να μεταβάλλουν την λειτουργικότητα της κλειστής συνάψεως και να προκαλέσουν ρήξιν του αιματοεγκεφαλικού φραγμού, επισωρεύοντες σοβαράς συνεπείας διά την περαιτέρω λειτουργικήν ακεραιότητα του κεντρικού νευρικού συστήματος. Εν μέσω αυτών ιδιαιτέραν βαρύτητα έχει η σεροτονίνη, η βραδυκινίνη, το αραχιδονικόν οξύ, το μονοξείδιον του αζώτου, αι ελεύθεραι ρίζαι του οξυγόνου, εκ δε των εξωγενώς χορηγουμένων παραγόντων τα υπέρτονα διαλύματα, η αμιτριπτυλίνη και οι α-αδρενεργικοί συναγωνισταί.
Ο ρόλος του αιματοεγκεφαλικού φραγμού εις τας ανοσοβιολογικάς αντιδράσεις
του κεντρικού νευρικού συστήματος και ιδίως εις την πολλαπλήν σκλήρυνσιν
Η μελέτη των πειραματικών προσπαθειών της ανοσοβιολογικής κινητοποιήσεως του κεντρικού νευρικού συστήματος, προς την κατεύθυνσιν της αναπτύξεως απλής ή υποτροπιαζούσης μορφής πειραματικής αλλεργικής εγκεφαλομυελίτιδος, κατέδειξεν ότι εκ των ουσιωδεστέρων σταθμών διά την ανοσοβιολογικήν ευαισθητοποίησιν του εγκεφάλου είναι η δίοδος ενεργοποιημένων λεμφοκυττάρων διά μέσου του αιματοεγκεφαλικού φραγμού.
Η δίοδος αύτη πραγματοποιείται διά μέσου αναπτύξεως σειράς μορίων προσφύσεως, μεταξύ των οποίων εντάσσονται αι ιντεγρίναι και ιδίως το υπέρβραδυ αντιγόνον τύπου 4 (VLA-4).
Τα ενδοθηλιακά κύτταρα εκ παραλλήλου, τελούντα υπό την επίδρασιν της γ ιντερφερόνης ή του παράγοντος νεκρώσεως των όγκων τύπου α (ΤΝF-α), διά της αναπτύξεως σειράς μορίων προσφύσεως23, ως είναι το αγγειακόν κυτταρικόν μόριον προσφύσεως (V-CAM) και τα αντιγόνα του μείζονος συστήματος ιστοσυμβατότητος τύπου ΙΙ, αποτελούν ευπρόσβλητον επιφάνειαν, διά της οποίας δύνανται να διέλθουν κυτταρικά στοιχεία24. Ούτω τα ενεργοποιημένα λεμφοκύτταρα, τα οποία εκφράζουν επί της επιφανείας των το υπέρβραδυ αντιγόνον τύπου 4 (VLA-4), δύνανται να συνδεθούν μετά των μορίων προσφύσεως της επιφανείας των ενδοθηλιακών κυττάρων καθισταμένης εφικτής της διόδου των κυττάρων διά μέσου των κλειστών συνάψεων.
Παραλλήλως προς την δίοδον των Τ λεμφοκυττάρων πραγματοποιείται δίοδος μονοκυττάρων και Β λεμφοκυττάρων, προερχομένων εκ δενδριτικών κυττάρων. Τα κύτταρα ταύτα, εισερχόμενα εις τον περιαγγειακόν χώρον, ευλόγως υφίστανται σειράν μορφολογικών και ανοσοβιολογικών τροποποιήσεων. Υφίστανται ενδείξεις ότι η διάνοιξις του αιματοεγκεφαλικού φραγμού συνδέεται μετά της παραγωγής αντιγόνου της κυτταρικής επιφανείας των ενδοθηλιακών κυττάρων, το οποίον ευλόγως καλείται αντιγόνον του ενδοθηλιακού φραγμού (ΕΒΑ), αντισώματα προς το οποίον είναι δυνατόν να διανοίξουν τας κλειστάς συνάψεις και να επιτρέψουν την επικοινωνίαν του αυλού των τριχοειδών μετά του νευροπιληματικού χώρου25.
Η δίοδος των κυτταρικών στοιχείων μετά από την πρόσφυσίν των επί των ενδοθηλιακών κυττάρων πραγματοποιείται συγχρόνως και εκ της επερχομένης αλλοιώσεως της βασικής μεμβράνης του τριχοειδούς. Ούτω διαπιστούται ότι μεταλλοπρωτεάσαι (ΜΜΡ) της βασικής μεμβράνης των τριχοειδών και ιδίως η ζελατινάση Β, αυξάνονται εις πυκνότητα εις τα τριχοειδή του κεντρικού νευρικού συστήματος κατά την διάρκειαν των ώσεων της πολλαπλής σκληρύνσεως επί του ανθρώπου26.
Αι μεταλλοπρωτεϊνάσαι, αι συνδεόμεναι μετά της δομής και λειτουργικότητος του αιματοεγκεφαλικού φραγμού περιλαμβάνουν την ζελατινάσην-Α (ΜΜΡ-2), αμφότεραι των οποίων δύνανται να αποδομήσουν το κολλαγόνον τύπου IV, το οποίον περιβάλλει το ενδοθήλιον των τριχοειδών του εγκεφάλου, την ζελατινάσην-Β (ΜΜΡ-9), την ματριλυσίνην (ΜΜΡ-7) και την στρωμελυσίνην (ΜΜΡ-3). Ολαι αύται αι μεταλλοπρωτεϊνάσαι, αι οποίαι περιέχουν Zn++ εις το μόριον αυτών, παράγονται υφ' όλων των κυτταρικών στοιχείων του κεντρικού νευρικού συστήματος, συμπεριλαμβανομένων και των νευρώνων.
Τα Τ λεμφοκύτταρα, απελευθερώνοντα ζελατινάση-Β, καθιστούν εφικτήν την δίοδον αυτών διά της βασικής μεμβράνης των τριχοειδών. Εκ παραλλήλου η ιντεγρίνη 1, παραγομένη υπό των ενεργοποιημένων λεμφοκυττάρων δύναται να συνδεθή, μετά του κολλαγόνου τύπου IV και κατ' επέκτασιν να καταστήση έτι ευχερεστέραν την δίοδον των λεμφοκυττάρων εις τον περιαγγειακόν χώρον27.
Η αναχαίτησις της δράσεως των μεταλλοπρωτεασών (ΜΜΡ), δύναται να πραγματοποιηθή υπό των ιστικών αναστολέων της δράσεως των μεταλλοπρωτεασών της βασικής μεμβράνης (ΤΙΜΡ), εκ των οποίων ο τύπου 1 (ΤΙΜΡ-1), κινητοποιούμενος υπό των κυττοκινών28 και ιδίως υπό του παράγοντος νεκρώσεως των όγκων τύπου α (ΤΝF-α), φαίνεται ότι διαδραματίζει σημαντικόν ρόλον επί της πολλαπλής σκληρύνσεως, ανευρισκόμενος εις το εγκεφαλονωτιαίον υγρόν των πασχόντων.
Η διαταραχή του αιματοεγκεφαλικού φραγμού επί της πολλαπλής σκληρύνσεως
και εισαγωγή θεραπευτικών σχημάτων διατηρήσεως αυτού
Εις την πολλαπλήν σκλήρυνσιν τόσον ενεργοποιημένα λεμφοκύτταρα, όσον και πρωτεϊνικοί παράγοντες24 φέρονται εκ του αυλού των τριχοειδών του κεντρικού νευρικού συστήματος προς τον περιαγγειακόν χώρον. Η ανεύρεσις της ζελατινάσης Α και Β εις το εγκεφαλονωτιαίον υγρόν των πασχόντων εκ πολλαπλής σκληρύνσεως καθιστά εμφανή την ενεργητικήν συμβολήν των ενεργοποιημένων λεμφοκυττάρων εις την διεργασίαν διεισδύσεως αυτών εντός του περιαγγειακού και του νευροπιληματικού χώρου ευρύτερον (Εικ.2).
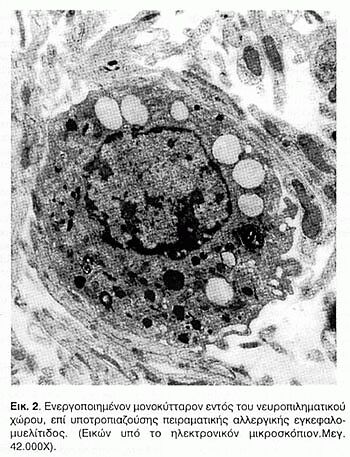
Η ιντερφερόνη-γ και η ιντερλευκίνη-12 διαδραματίζουν σημαντικόν ρόλον ως προφλεγμονώδεις παράγοντες, συμβάλλοντες εις την διάνοιξιν του αιματοεγκεφαλικού φραγμού29.
Ο παράγων νεκρώσεως των όγκων τύπου α (ΤΝF-α) και η ιντερλευκίνη-1 αυξάνουν την ρήξιν των κλειστών συνάψεων επί οξειδωτικής καταπονήσεως, ενώ η ιντερλευκίνη-6 δεν μεταβάλλει την ακεραιότητα του αιματοεγκεφαλικού φραγμού ούτε προσαυξάνει την ρήξιν αυτού επί οξειδωτικής καταπονήσεως.
Η συνυπάρχουσα οξειδωτική καταπόνησις, συνοδευομένη υπό του σχηματισμού υπεροξειδικών σωμάτων και μονοξειδίου του αζώτου (ΝΟ), συμβάλλει εις την περαιτέρω διάνοιξιν του αιματοεγκεφαλικού φραγμού και την ολοκλήρωσιν της διεργασίας διόδου παραγόντων διά των ανοικτών πλέον "κλειστών συνάψεων". Η κυτταροτοξικότης εξ υπερεργείας, συνδεομένη μετά της επιμόνου δράσεως του γλουταμινικού οξέος επί των NMDA υποδοχέων, οδηγούσα πολλάκις εις την οξειδωτικήν καταπόνησιν30, δύναται να συμβάλη εις την περαιτέρω διάνοιξιν του αιματοεγκεφαλικού φραγμού και να διαδραματίση ρόλον τινα εις την παθογένειαν της πολλαπλής σκληρύνσεως31.
Διά των συγχρόνων νευροαπεικονιστικών μεθόδων, τόσον διά της ποζιτρονικής τομογραφίας32 όσον ιδίως διά της μαγνητικής τομογραφίας και της εφαρμογής της τεχνικής FLAIR (fluid attenuated inversion recover) και της μαγνητικής φασματοσκοπικής αναλύσεως καθίσταται αντιληπτόν ότι επί της πρώτης φαινομενολογικής εκδηλώσεως της πολλαπλής σκληρύνσεως ο αιματοεγκεφαλικός φραγμός εμφανίζει ρήξιν, η οποία παραμένει ως έχει επί 6 ώρας έως 7 ημέρας. Ευεργετικήν επίδρασιν εις την αποκατάστασιν του αιματοεγκεφαλικού φραγμού ασκούν τα στεροειδή, η χορήγησις των οποίων αιτιολογείται πλήρως κατά την έναρξιν της νόσου33.
Εκ παραλλήλου η αντιρρόπησις της δράσεως της γ-ιντερφερόνης δύναται να ευνοήση την διατήρησιν του αιματοεγκεφαλικού φραγμού και να ασκήση ευεργετικήν επίδρασιν επί της πολλαπλής29 σκληρύνσεως. Εκ παραλλήλου η χορήγησις β-ιντερφερόνης αναστέλλει την δράσιν της ζελατινάσης -Β (ΜΜΡ-9), η δε χορήγησις της ιντερφερόνης βήτα-1α εις την μορφήν της πολλαπλής σκληρύνσεως, την χαρακτηριζομένην υπό υφέσεων και εξάρσεων, επιδρά κατασταλτικώς και επί της ματριλυσίνης (ΜΜΡ-7), διατηρώσα ως εκ τούτου την στεγανότητα του αιματοεγκεφαλικού φραγμού34. Εκ παραλλήλου ο αυτός τύπος της ιντερφερόνης κινητοποιεί τους ιστικούς αναστολείς της δράσεως των μεταλλοπρωτεασών της βασικής μεμβράνης (ΤΙΜΡ) και ιδίως τον τύπον 1 (ΤΙΜΡ-1), με αποτέλεσμα να τροποποιή τον λόγον ΜΜΡ/ ΤΙΜΡ εκ της πρωτεολυτικής σχέσεως προς την αντιπρωτεολυτικήν τοιαύτην, γεγονός το οποίον αναχαιτίζει την δίοδον των ενεργοποιημένων λεμφοκυττάρων διά του αιματοεγκεφαλικού φραγμού34.
Εκ παραλλήλου η εφαρμογή νευροτροφινών και ιδίως του παράγοντος BDNF35 φαίνεται ότι συμβάλλει εις την αποκατάστασιν του ραγέντος αιματοεγκεφαλικού φραγμού, ως τούτο καταδείχθη επί τραυματικών βλαβών του νωτιαίου μυελού, δυνάμενος εις το μέλλον να χορηγηθή επί της αρχικής εκδηλώσεως της πολλαπλής σκληρύνσεως.
Συγχρόνως η εφαρμογή αναστολέων της σερινικής πρωτεάσης δύναται να συμβάλη εις την αποκατάστασιν του αιματοεγκεφαλικού φραγμού, οσάκις ούτος διανοίγεται υπό την επίδρασιν του παράγοντος νεκρώσεως των όγκων τύπου α (ΤΝF-α)36. Οι αναστολείς επίσης της φωσφοδιεστεράσης τύπου IV, δύνανται να επενεργήσουν ευεργετικώς συμβάλλοντες εις την αποκατάστασιν του αιματοεγκεφαλικού φραγμού, ως τούτο κατεδείχθη επί του προτύπου της πειραματικής αυτοανοσοβιολογικής εγκεφαλομυελίτιδος37.
Το γεγονός ότι η οξειδωτική καταπόνησις συμβάλλει εις την διάνοιξιν του αιματοεγκεφαλικού φραγμού38, οδηγεί εις την σκέψιν ότι υψηλά δοσολογικά σχήματα βιταμινών Ε και C, δύνανται να συμβάλουν ευεργετικώς επί της πολλαπλής σκληρύνσεως. Το αυτό ισχύει και διά την αύξησιν των επιπέδων του ουρικού οξέος, διά της χορηγήσεως ινοσίνης, δεδομένου ότι αυξανομένων των επιπέδων του ουρικού οξέος ελαττούνται τα επίπεδα του υπεροξυνιτρίτου.
Μεγαλυτέρας ακτίνας ελπίδος θα επιτρέψη ίσως να διαλάμψουν η εφαρμογή των ανταγωνιστών των παραγόντων της κυτταρικής προσφύσεως, ως είναι οι παράγοντες LFA-1 και VLA-4 και αι ιντεγρίναι, διά των οποίων θα απεφεύγοντο αι προσφύσεις των ενεργοποιημένων λεμφοκυττάρων επί των ενδοθηλιακών κυττάρων των τριχοειδών των εγκεφαλικών αγγείων και η εν συνεχεία είσοδος αυτών εντός του περιαγγειακού χώρου, γεγονός το οποίον ακινητοποιεί τα περαιτέρω δραματικότερα στάδια της ανοσοβιολογικής αντιδράσεως, η οποία καταλήγει εις την καταστροφήν της μυελίνης και εις την αξονικήν βλάβην39.
Συγχρόνως διαιτητικά ή φαρμακολογικά σχήματα παροχής φλαβινοειδών40 ήτοι ανθοκυανοσιδών, προανθολυανοσιδών και προκυανιδολικών ολιγομερών (PCO) δύναται να συμβάλη εις την ισχυροποίησιν του αιματοεγκεφαλικού φραγμού41, καθ'όσον τα φλαβινοειδή αφ'ενός μεν συνδεόμενα μετά των μεταλλοπρωτεασών (ΜΜΡ) αδρανοποιούν ταύτας, συμβάλλοντα εις την διατήρησιν της βασικής μεμβράνης των τριχοειδών42, αφ΄ετέρου δε ως ισχυροί αντιοξειδωτικοί παράγοντες δύνανται να αντιρροπήσουν την οξειδωτικήν καταπόνησιν και να αποφευχθή ούτως η συνεπεία αυτής διαταραχή της ακεραιότητος του αιματοεγκεφαλικού φραγμού.
Εν κατακλείδι η αναγνώρισις ότι η ρήξις του αιματοεγκεφαλικού φραγμού αποτελεί κεφαλαιώδες φαινόμενον διά την έναρξιν των ανοσοβιολογικών διεργασιών, αι οποίαι εν τω συνόλω των θα στοιχειοθετήσουν το παθογενετικόν περίγραμμα της πολλαπλής σκληρύνσεως, οδηγεί εις την σκέψιν ότι η θεραπευτική αντιμετώπισις της νόσου θα πρέπη νά άρχεται το ταχύτερον δυνατόν, συνισταμένη αρχικώς εκ διαιτητικών και φαρμακευτικών παραγόντων, οι οποίοι θα αποκαταστήσουν ταχέως την ανατομικήν και λειτουργικήν ακεραιότητα του αιματοεγκεφαλικού φραγμού και θα εγγυηθούν την στεγανότητα αυτού ώστε ταχέως να περιορισθή η διείσδυσις ενεργοποιημένων λεμφοκυττάρων και κυττοκινών εντός του περιαγγειακού χώρου και να περιχαρακωθή η έκτασις και η διάρκεια της ανοσοβιολογικής αντιδράσεως.
ΒΙΒΛΙΟΓΡΑΦΙΑ