|
|||
|
|||
Συγκριτική μελέτη των διακυμάνσεων του λόγου των CD4/CD8 λεμφοκυττάρων
σε ασθενείς με σκλήρυνση κατά πλάκας με τη μορφή των υφέσεων-εξάρσεων
υπό θεραπεία με Αζαθειοπρίνη ή Ιντερφερόνη βήτα 1-α
ΖΑΦΕΙΡΟΠΟΥΛΟΣ Α., ΞΑΦΕΝΙΑΣ Δ., ΖΑΦΕΙΡΟΠΟΥΛΟΣ Κ., ΒΑΣΙΛΑΚΗ Ο., ΞΑΦΕΝΙΑΣ Α.,
ΚΟΥΦΟΓΙΑΝΝΗΣ Δ., ΤΣΑΒΔΑΡΙΔΟΥ Β., ΑΓΓΟΥΡΙΔΑΚΗ Χ., ΔΗΜΗΤΡΙΑΔΗΣ Ε.Α.
Α' Πανεπιστημιακή Νευρολογική Κλινική, Γενικό Περιφερειακό Νοσοκομείο ΑΧΕΠΑ, Θεσσαλονίκη
Περίληψη
Είναι γνωστό ότι, τα Τ-λεμφοκύτταρα, διαδραματίζουν ένα σημαντικό και καθοριστικά ρυθμιστικό ρόλο, στην πορεία των αυτοάνοσων νοσημάτων. Στηριζόμενοι σε ποικίλες ενδείξεις που ενισχύουν την άποψη της ανοσοβιολογικής παθογένειας της σκλήρυνσης κατά πλάκας (MS), αξιολογήσαμε τις διακυμάνσεις των επιπέδων του λόγου των υποπληθυσμών των T-λεμφοκυττάρων CD4/CD8 στο περιφερικό αίμα ασθενών που έπασχαν από MS με την μορφή των υφέσεων και εξάρσεων για περίοδο ενός έτους. Οι ασθενείς βρισκόταν σε θεραπεία είτε με ανοσοκατασταλτικούς παράγοντες, την αζαθειοπρίνη (ΑΖ 1η ομάδα) ,είτε με ανοσορυθμιστικούς παράγοντες, την ιντερφερόνη Β (IFN β-1α 2η ομάδα). Τα αποτελέσματα μας έδειξαν ότι η σχέση του λόγου των υποπληθυσμών CD4/CD8 λεμφοκυττάρων εμφανίζεται σε μικρό ποσοστό σε παθολογικές διακυμάνσεις ακόμα και στις περιόδους έξαρσης της νόσου, στην ομάδα της IFN β-1α ενώ στην ομάδα της ΑΖ οι ασθενείς εμφάνισαν υψηλότερο ποσοστό παθολογικών διακυμάνσεων του λόγου των CD4/CD8 και ιδιαίτερα στις εξάρσεις της νόσου. Παρόλα αυτά η στατιστική μελέτη μεταξύ των δύο ομάδων όσον αφορά στις εξάρσεις της νόσου και στις παθολογικές τιμές του λόγου των CD4/CD8 λεμφοκυττάρων δεν αποκάλυψε στατιστικά σημαντική διαφορά.
Λέξεις κλειδιά: Πολλαπλή σκλήρυνση, CD4/CD8, αζαθειοπρίνη, ιντερφερόνη βήτα 1-α.
Εισαγωγή
Η επικρατέστερη αιτιοπαθογενετική θεωρία της πολλαπλής σκλήρυνσης (MS) είναι η αυτοανοσοβιολογική. Κατ' αυτήν, υποστηρίζεται ότι στην παθολογία της νόσου συμμετέχουν αυτοανοσομεσολαβούντες μηχανισμοί1. Μια πληθώρα από κλινικά και πειραματικά δεδομένα που υποστηρίζουν την ανοσοβιολογική φύση της νόσου2, στηρίζουν τη χορήγηση ανοσοκυτταροτοξικών ή ανοσορρυθμιστικών παραγόντων όσο αφορά στη θεραπευτική αντιμετώπιση αυτής3 .Έτσι μέχρι σήμερα έχουν χρησιμοποιηθεί τα κορτικοστεροειδή και η ACTH, τα άμεσα κυτταροτοξικά φάρμακα, όπως η αζαθειοπρίνη4, η κυκλοφοσφαμίδη5 και η κυκλοσπορίνη Α6 ,καθώς και μία πληθώρα από άλλους παράγοντες οι οποίοι μπορούν να επηρεάσουν ευνοϊκά την ανοσολογική αντίδραση του αρρώστου, όπως η IFN-β- 1α7,η πλασμαφαίρεση8, το συνθετικό πολυπεπτίδιο Copolymer 19, η ολική ακτινοβόληση του λεμφοποιητικού συστήματος10, η θυμεκτομή11 και τα μονοκλωνικά αντισώματα12.
Αναφορές για την κλινική αποτελεσματικότητα της αζαθειοπρίνης (ΑΖ) στη θεραπεία της MS είναι αλληλοσυγκρουόμενες και παρά την εγγενή δυσκολία στην εκτίμηση των κλινικών αποτελεσμάτων υπάρχουν αναφορές που συνηγορούν στο ότι η μακροχρόνια χορήγηση της ΑΖ δεν ελαττώνει τον αριθμό ή τη βαρύτητα των ώσεων ούτε αναχαιτίζει την εξέλιξη της νόσου, τόσο στους ασθενείς με εξάρσεις και υφέσεις, όσο και στους ασθενείς με χρόνια προοδευτικά εξελισσόμενη μορφή της νόσου. Άλλες μελέτες αναφέρουν σημαντικό περιορισμό της συχνότητας των εξάρσεων ή και πλήρη εξάλειψη αυτών με τη χορήγηση της ΑΖ σε ασθενείς με εξάρσεις και υφέσεις σε σύγκριση με εκείνους που δεν χορηγήθηκε ΑΖ. Ο Yudkin και οι συνεργάτες του σε μία εκτεταμένη μετα-ανάλυση που αφορούσε την αποτελεσματικότητα της ΑΖ σε 7 εργασίες (2 μονές και 5 διπλές τυφλές) διαπίστωσαν ότι δεν υπάρχει καμία διαφορά μεταξύ των ασθενών που θεραπεύονταν με ΑΖ και εκείνων των ασθενών στους οποίους χορηγούνταν placebo, στην αύξηση της βαθμολογίας της κλίμακας EDSS (expanded disability status scale) στον πρώτο χρόνο θεραπείας, ενώ για το δεύτερο χρόνο διαπίστωσε μια μικρή μείωση της βαθμολογίας αυτής στην ομάδα της ΑΖ(0,22 βαθμούς) και για τον τρίτο χρόνο 0,4 βαθμούς, μια πτώση που δεν θεωρείται στατιστικά και κλινικά σημαντική. Στην ίδια ανάλυση οι ερευνητές παρόλα αυτά διαπίστωσαν ότι στους ασθενείς που βρίσκονταν σε αγωγή με ΑΖ περιορίζεται σημαντικά ο κίνδυνος υποτροπής με μία πιθανότητα για μεν τον πρώτο χρόνο θεραπείας 1,51 φορές μεγαλύτερη, μετά τα δύο χρόνια 2,4 φορές και μετά τα 3 χρόνια 1,97 φορές, οι ασθενείς αυτοί να παραμείνουν απαλλαγμένοι από εξάρσεις. Πρόσφατα διαπιστώθηκε ότι η IFNβ-1α μπορεί να περιορίσει τη συχνότητα των εξάρσεων της νόσου με χωρίς ιδιαίτερης βαρύτητας παρενέργειες. Η ευεργετική δράση της IFN-B στην MS φαίνεται ότι εξαρτάται από την ικανότητα αυτής είτε να καταστέλλει τη φάση ενεργοποίησης, είτε να περιορίζει τη φάση της ανοσιακής δραστηριότητας, είτε να ενισχύει τους μηχανισμούς καταστολής της ειδικής ανοσιακής απάντησης και τέλος να εκδηλώνει μία πλέον συνδυασμένη δράση στις τρεις παραπάνω επιμέρους φάσεις. Ο λόγος CD4/CD8 φαίνεται να σχετίζεται άμεσα με την εξέλιξη της νόσου και ιδιαίτερα με τις εξάρσεις αυτής. Έτσι, ένας καλός δείκτης της αποτελεσματικότητας ενός φαρμακευτικού παράγοντα, είναι η συσχέτιση του λόγου των CD4/CD8 με την κλινική εικόνα. Ο σκοπός της εργασίας αυτής είναι η αξιολόγηση της θεραπευτικής αποτελεσματικότητας της ΑΖ σε σχέση με αυτήν της IFN-B με την αξιολόγηση τόσον κλινικών δεικτών(κλίμακα EDSS) όσον και βιολογικών παραμέτρων
Υλικό-μέθοδος
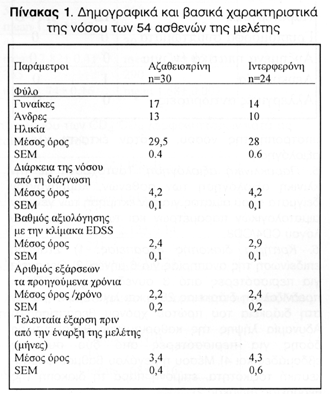

Αποτελέσματα
Κατά τη διάρκεια της 12μηνης παρακολούθησης έγιναν συνολικά 290 αξιολογήσεις (τόσο κλινικές όσο και εργαστηριακές) στους ασθενείς της ομάδας της IFN-B. Από αυτές δύο ήταν εκτός μηνιαίου προγραμματισμού, λόγω δύο εξάρσεων της νόσου στα μεσοδιαστήματα της μηνιαίας αξιολόγησης. Όσον αφορά στην ομάδα της ΑΖ, έγιναν 365 συνολικά αξιολογήσεις, από τις οποίες 5 ήταν εκτός μηνιαίου προγραμματισμού (πίνακας 3). Στην ομάδα της IFN-B από τις 290 αξιολογήσεις διαπιστώσαμε συνολικά 19 εξάρσεις της νόσου ενώ οι υπόλοιπες 271 αξιολογήσεις συνέπεσαν σε περιόδους ύφεσης. Στην ομάδα της ΑΖ από τις 365 συνολικά αξιολογήσεις διαπιστώθηκαν 32 εξάρσεις της νόσου ενώ οι υπόλοιπες 333 αξιολογήσεις έγιναν σε περίοδο ύφεσης. Όσον αφορά στις διακυμάνσεις των επιπέδων του λόγου CD4/CD8 διαπιστώσαμε συνολικά 30 παθολογικές τιμές και 260 φυσιολογικές στην ομάδα της IFN-B με μέσο όρο 2,24 0,32 και 1,64 0,04 αντίστοιχα, ενώ στην ομάδα της ΑΖ διαπιστώσαμε 41 παθολογικές και 324 φυσιολογικές τιμές με μέσο όρο 2,82±0,41 και 1,59±0,03 αντίστοιχα. Από τις τιμές αυτές όσον αφορά στις περιόδους έξαρσης διαπιστώσαμε για μεν την ομάδα της INF-B 13 φυσιολογικές και 6 παθολογικές τιμές του λόγου των CD4/CD8 με μέσο όρο 1,68±0,16 και 2,36±0,19 αντίστοιχα, ενώ στην ομάδα της ΑΖ διαπιστώσαμε 11 φυσιολογικές και 21 παθολογικές τιμές με μέσο όρο 1,71±0,004 και 2,92±0,18 αντίστοιχα. Στις περιόδους ύφεσης της νόσου διαπιστώσαμε στην ομάδα της IFN-B 247 φυσιολογικές τιμές και 24 παθολογικές με μέσο όρο 1,61±0,2 και 2,12±0,14 αντίστοιχα ενώ στην ομάδα της ΑΖ διαπιστώσαμε 313 φυσιολογικές και 20 παθολογικές με μέσο όρο 1,52±0,17 και 2,59±0,36 αντίστοιχα (πίνακες 4,5).
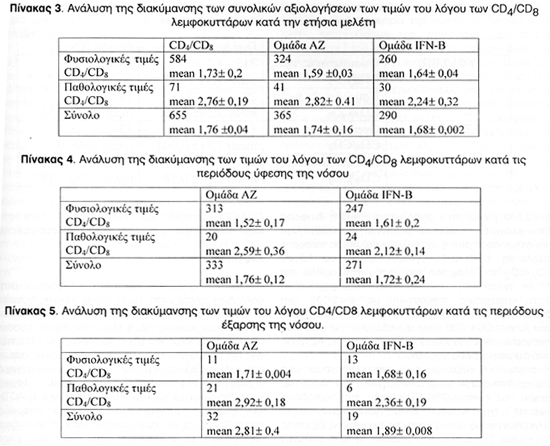
Από την στατιστική ανάλυση των αποτελεσμάτων μας δεν παρατηρήσαμε στατιστικά σημαντική διαφορά του λόγου των CD4/CD8 λεμφοκυττάρων μεταξύ των εξάρσεων και υφέσεων της νόσου ανάμεσα στις δύο ομάδες (p=0,29) (πίνακας 6). Και στις δύο ομάδες παρατηρήθηκαν υψηλότερες τιμές του λόγου CD4/CD8 στις περιόδους έξαρσης της νόσου από ότι στις υφέσεις αυτής. Ιδιαίτερα στην ομάδα της ΑΖ η διαφορά αυτή ήταν υψηλά στατιστικά σημαντική (p<0,0001) ενώ στην ομάδα της IFN-B η διαφορά ήταν ελάχιστα στατιστικά σημαντική (p<0,05). Άξιο παρατήρησης ήταν η σε πολύ μεγαλύτερο ποσοστό εμφάνιση των παθολογικών τιμών του λόγου CD4/CD8 στις εξάρσεις της νόσου στην ομάδα της ΑΖ σε σχέση με αυτήν της INF-B. Η διαφορά αυτή ήταν στατιστικά σημαντική με p<0,005 μια διαπίστωση που υποδηλώνει ότι οι παθολογικές τιμές του λόγου CD4/CD8 που συνοδεύουν τις εξάρσεις της νόσου είναι συχνότερες στην ομάδα της ΑΖ παρά από ότι στην ομάδα της IFN-B.
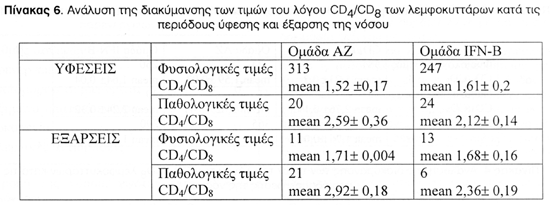
Η στατιστική ανάλυση των αποτελεσμάτων μας επίσης αποκάλυψε ότι οι διακυμάνσεις των απόλυτων τιμών του λόγου CD4/CD8 κατά τις περιόδους ύφεσης της νόσου είναι μικρότερες όταν συγκρίνονται με αυτές κατά τις περιόδους έξαρσης της νόσου. Πιο ειδικά στην ομάδα της ΑΖ η απόλυτη τιμή του λόγου CD4/CD8 είναι μεγαλύτερη στις περιόδους έξαρσης της νόσου από ότι στις περιόδους ύφεσης αυτής με μία λίαν στατιστικά σημαντική διαφορά (p<0,0001) ενώ αντίθετα μεταξύ των περιόδων ύφεσης και έξαρσης στην ομάδα της IFN-B η διαφορά των απολύτων τιμών του λόγου CD4/CD8 δεν παρουσιάζει στατιστικά αξιόλογη διαφορά (p=0,038).
Επιπρόσθετα η στατιστική ανάλυση των αποτελεσμάτων μας, έδειξε ότι δεν υπάρχει στατιστικά σημαντική διαφορά μεταξύ των παθολογικών και των φυσιολογικών τιμών του λόγου CD4/CD8 στις περιόδους έξαρσης της νόσου μεταξύ των δύο ομάδων. Αντίθετα υπάρχει λίαν στατιστικά σημαντική διαφορά μεταξύ των παθολογικών και φυσιολογικών τιμών του λόγου CD4/CD8 στις περιόδους ύφεσης και στις δύο ομάδες. Τέλος δεν παρατηρήσαμε στατιστικά σημαντική διαφορά μεταξύ των φυσιολογικών και παθολογικών τιμών του λόγου CD4/CD8 μεταξύ των δύο ομάδων ούτε στις περιόδους έξαρσης ούτε και στις περιόδους ύφεσης.
Συζήτηση
Ο σκοπός της ανοσοκατασταλτικής θεραπείας στην πολλαπλή σκλήρυνση είναι: (α) η ταχύτερη ανάρρωση από κάθε ώση, (β) η ελάττωση του αριθμού των μελλοντικών ώσεων, (γ), η ελάττωση της επισυσσώρευσης αναπηρίας και (δ), η πρόληψη της μετάπτωσης της νόσου από τη μορφή των υφέσεων-εξάρσεων στη χρόνια εξελικτική μορφή. Έτσι στη μέχρι σήμερα ισχύουσα θεραπευτική προσπάθεια, αρχικά χρησιμοποιούνται τα κορτικοστεροειδή και η ACTH και όταν το αποτέλεσμα δεν είναι επαρκές, προστίθενται οι ανοσοκατασταλτικοί-κυτταροτοξικοί παράγοντες, με επικράτηση στον ευρωπαϊκό χώρο της ΑΖ και πρόσφατα της INF7,14,18.
Οι κλινικές αναφορές για τη χρήση της ΑΖ είναι αλληλοσυγκρουόμενες, όσον αφορά στη δραστικότητά της, και παρά την εγγενή δυσκολία στην εκτίμηση των κλινικών αποτελεσμάτων19,20, υπάρχουν αναφορές όπου τονίζεται ότι η μακροχρόνια χορήγηση ΑΖ, δεν ελαττώνει τον αριθμό ή τη σοβαρότητα των ώσεων, ούτε συγκρατεί ούτε αναχαιτίζει την εξέλιξη της νόσου, τόσο για τους ασθενείς με εξάρσεις και υφέσεις, όσο και για τους χρόνιους προοδευτικά εξελισσόμενους ασθενείς21,22. Άλλες έρευνες αναφέρουν μεγάλη ελάττωση του ρυθμού των εξάρσεων ή και εξάλειψη αυτών με τη χορήγηση ΑΖ στους ασθενείς με εξάρσεις και υφέσεις, σε σύγκριση με εκείνους που δεν παίρνουν ΑΖ4,23-25,27. Όσον αφορά στους ασθενείς με τη χρόνια προοδευτική μορφή, άλλοι μεν αναφέρουν κάποια ευνοϊκή επίδραση25-28 ενώ άλλοι δεν παρατηρούν καμία αλλαγή4,23. Επίσης αναφέρεται ένας επιβραδυνόμενος ρυθμός επιδείνωσης των VEP και SSEP μαζί με μία μικρή βελτίωση της κατάστασης αναπηρίας κατά Kurtzke.
Οι γνώσεις μας όσον αφορά στη δράση της IFN-B στους ασθενείς με MS με τη μορφή των υφέσεων και εξάρσεων παραμένουν αδιευκρίνιστες. Φαίνεται ότι η IFN-B παρουσιάζει μια σειρά από αποτελέσματα επάνω στην άνοσοβιολογική αλυσίδα όπως: α). ελάττωση της σύνθεσης της IFN-B , β). ενίσχυση της δραστηριότητας των κατασταλτικών κυττάρων και γ). ελάττωση της ρυθμιστικής δράσης της τάξης II MHC στη μεσολαβητική έκφραση της IFN-B μέσω αντιγονικά εμφανιζομένων κυττάρων. Επίσης η IFN-B εμφανίζει αντιϊκή δραστηριότητα, μειώνει τη ρυθμιστική δραστηριότητα του νεκρωτικού των όγκων παράγοντα (TNF) και πιθανόν ενεργοποιεί την παραγωγή των ενδογενών του φλοιού των επινεφριδίων στεροειδών στους ασθενείς με φλεγμονώδη αντίδραση από την τοπική χορήγησή της29,30.
Όσον αφορά στα Τ-Λεμφοκύτταρα, είναι πολύ πιθανόν να συμμετέχουν στο μηχανισμό της αυτοάνοσης κατάσπασης του ελύτρου της μυελίνης και στις απομυελινωτικές βλάβες βρίσκονται κυρίως CD4, CD8 και Ια+ κύτταρα (μακροφάγα και Β-λεμφοκύτταρα). Διάφορες μελέτες έχουν δείξει μια ελάττωση του αριθμού και μία ατελή λειτουργική δραστηριότητα των CD8 λεμφοκυττάρων (suppressor) στους MS ασθενείς, ενώ τα CD4 λεμφοκύτταρα (helper) βρίσκονται σε μία ενεργοποιημένη κατάσταση, με περισσότερα επιφανειακά αντιγόνα ενεργοποίησης, έναντι φυσιολογικών μαρτύρων. Έτσι η σχέση CD4/CD8 φαίνεται να είναι αυξημένη στις εξάρσεις της κλινικής δραστηριότητας της νόσου, που οφείλεται κυρίως στην ελάττωση των CD8 και συγχρόνως τα CD4 βρίσκονται σε ενεργοποιημένη κατάσταση, σε αντίθεση με τα λειτουργικώς ατελή CD8. Οι μεταβολές στις σχέσεις CD4/CD8 έχουν συσχετιστεί θετικά με τις κλινικές εξάρσεις όσον αφορά στους ασθενείς με εξάρσεις και υφέσεις, ενώ δεν έχει παρατηρηθεί κάποια συσχέτιση στους χρόνιους προοδευτικά εξελισσόμενους ασθενείς31-39.
Την τελευταία δεκαετία πολλοί ερευνητές αναφέρουν μια σημαντική αύξηση του λόγου CD4/CD8 με μία εκατοστιαία μείωση των CD8+Τ-λεμφοκυττάρων τόσο στο περιφερικό αίμα όσο και στο ENΥ των ασθενών που πάσχουν από MS και βρίσκονται σε περίοδο έξαρσης της νόσου. Άλλοι εκφράζουνε μία αντίθετη άποψη αδυνατώντας να βρουν οποιαδήποτε σημαντική συσχέτιση μεταξύ τροποποιήσεων στους T-κυτταρικούς πληθυσμούς και στην κλινική πορεία της νόσου. Ο Selmay et al 1986, περιγράφουν μια σημαντική ποσοστιαία αύξηση των Tac+ κυττάρων στο περιφερικό αίμα των ασθενών με έξαρση συγκρινόμενα με αυτά σε περιόδους ύφεσης. Πάντως άξιο παρατήρησης είναι το γεγονός ότι οι περισσότερες από τις μελέτες αναφέρονται σε περιορισμένο αριθμό ασθενών και σε μικρό χρονικό διάστημα μελέτης15,39,40. Πρόσφατα ο Battistini L. και οι συνεργάτες του συνέκριναν την διάθεση πρόσφυσης των CD4+ και CD8+ λεμφοκυττάρων κάτω από φυσιολογικές συνθήκες σε μη-θεραπευμένους ασθενείς που έπασχαν από MS με τη μορφή των εξάρσεων-υφέσεων στη φάση έξαρσης της νόσου και σε υγιείς εθελοντές. Διαπίστωσαν ότι στους ασθενείς με πολλαπλή σκλήρυνση τα CD8+ και όχι τα CD4+T-λεμφοκύτταρα εκδήλωναν μία αυξημένη επιβράδυνση της ροής στα φλεγμονώδη αγγεία των πειραματόζωων. Επιπρόσθετα τα CD8+ και όχι τα CD4+ των ασθενών με MS έδειξαν μία αυξημένη επιβράδυνση επάνω στη β-σελεκτίνη in vitro. Η χορήγηση anti p-selectin γλυκοπρωτείνης έδειξε έναν δραματικό αποκλεισμό της δέσμευσης των CD8 κυττάρων στα αγγεία του εγκεφάλου των ασθενών με MS. H PSGL-1 (anti-P-selectin lipoprotein legend-1) φαίνεται να παριστάνει ένα νέο φαρμακευτικό παράγοντα ο οποίος παρεμποδίζει την εκλεκτική είσοδο των CD8 λεμφοκυττάρων κατά τη διάρκεια μίας πρώιμης φάσης φλεγμονής. Τα μόρια πρόσφυσης των αγγείων (VCAM-1) και όχι η PSGL-1 είναι κριτικής σημασίας για την πρόσφυση των CD4+ κυττάρων στους ασθενείς με MS, ένας μηχανισμός που είναι απαραίτητος για την εκδήλωση των εξάρσεων της MS στους ασθενείς με εξάρσεις-υφέσεις.41
Σημαντικός αριθμός από προηγηθείσες μελέτες έρχεται σε πλήρη συμφωνία με πρόσφατη έρευνα του Crucian B et al 1995, οι οποίοι μελέτησαν τον λόγο CD4/CD8 στο περιφερικό αίμα ασθενών με MS και διαπίστωσαν έναν αυξημένο λόγο των CD4/CD8 ο οποίος πρωταρχικά οφείλεται στην ελάττωση των CD8+ T-κυττάρων. Πιο ειδικά στους ασθενείς με MS και στις εξάρσεις της νόσου παρατηρήθηκε μία σημαντική ελάττωση των επιπέδων των προδρόμων κατασταλτικών (CD28-) υποπληθυσμών των CD8+ T-κυττάρων συγκρινόμενα με εκείνα της ομάδας ελέγχου, αλλά με φυσιολογικά επίπεδα των κυτταροτοξικών (CD28+) υποπληθυσμών των CD8+ T-κυττάρων. Τα ανωτέρω δεδομένα υποδηλώνουν ότι στους ασθενείς με MS δεν εμφανίζεται μία συνολική ελάττωση των CD8+T-κυττάρων αλλά έχουμε μία ελάττωση ενός συγκεκριμένου τύπου υποπληθυσμού των CD8+T-κυττάρων των προδρόμων κατασταλτικών μόνο και φυσιολογικά επίπεδα των κυτταροτοξικών. Επίσης στους ασθενείς με MS διαπιστώνεται μία σημαντική αύξηση των μνημονικών (CD45RO+) των CD4+T-κυττάρων και αυτή η αύξηση εξισορροπείται με μία ανάλογη ελάττωση των Naive (CD45RA+) T-κυττάρων στο περιφερικό αίμα. Επίσης οι Sculina C. και οι συνεργάτες του μελέτησαν την πορεία της ενεργοποίησης των επιφανειακών υποδοχέων των T-λεμφοκυττάρων τόσο στον εγκέφαλο, στο ΕΝΥ, όσο και στο περιφερικό αίμα σε δύο ασθενείς με MS οι οποίοι είχαν διαγνωστεί με βιοψία εγκεφάλου λόγω άτυπων κλινικών εκδηλώσεων. Ορισμένα από τα CD8 κύτταρα διασποράς παρατηρήθηκαν σε ορισμένα CD38 αιματικά κύτταρα υποθέτοντας ότι ακόμα και αυτά ήταν ενεργοποιημένα με τελική διαπίστωση ότι ορισμένα από τα CD8+T-λεμφοκύτταρα που διαπέρασαν στον εγκέφαλο παραμένουν για >5 χρόνια και στο ΕΝΥ και στο περιφερικό αίμα ενεργοποιημένα και αποτελούν καλό δείκτη για την πορεία της νόσου.15,42
Η ανάλυση των αποτελεσμάτων μας παρά το ότι δεν αποκάλυψε ιδιαίτερη στατιστικά σημαντική διαφορά μεταξύ των εξάρσεων και υφέσεων στις δύο ομάδες έδειξε υψηλότερες τιμές του λόγου CD4/CD8 στις εξάρσεις της νόσου και στις δύο ομάδες αλλά για μεν την ομάδα της IFN-B η διαφορά ήταν ελάχιστα στατιστικά σημαντική (p<0.05) ενώ στην ομάδα της AZ η διαφορά αυτή ήταν πάρα πολύ στατιστικά σημαντική (p<0.0001). Επίσης η εμφάνιση σε υψηλότερο ποσοστό των παθολογικών τιμών του λόγου CD4/CD8 και των εξάρσεων της νόσου στην ομάδα της AZ από ότι της IFN-B με στατιστικά σημαντική διαφορά (p<0.005) υποδηλώνει ότι οι παθολογικές τιμές του λόγου CD4/CD8 που συνοδεύουν τις εξάρσεις της νόσου είναι συχνότερες στην ομάδα της AZ από ότι στην ομάδα της IFN-B.
Συμπερασματικά γίνεται έκδηλο ότι η θεραπευτική παρέμβαση της IFN-B στους ανοσοβιολογικούς μηχανισμούς των ασθενών με MS και με την μορφή των υφέσεων και εξάρσεων είναι πιο ισχυρή από εκείνη της AZ, και ιδιαίτερα στη διακίνηση των επιπέδων του λόγου CD4/CD8, ο οποίος θεωρείται ένας ισχυρός δείκτης της ανοσοβιολογικής δραστηριότητας, ενισχύοντας την άποψη ότι η θεραπευτική παρέμβαση της IFN-B αποτελεί έναν ισχυρό θεραπευτικό παράγοντα στην αντιμετώπιση της κλινικής πορείας της MS. Παρόλα αυτά, πρόσφατη μελέτη συγχορήγησης IFN-B και AZ σε ασθενείς που πάσχουν από MS έδειξε καλύτερη κλινική πορεία και βελτίωση της μαγνητικής απεικόνισης των ασθενών σε σύγκριση με άλλες μελέτες μονοθεραπείας είτε με ΑΖ είτε με IFN-B.43
ΒΙΒΛΙΟΓΡΑΦΙΑ